Fagfellevurdert

Pasientspesifikk funksjonsskala hos pasienter med akutt hjerneslag. En prospektiv kohortstudie
Vitenskapelig artikkel
Tonje Kristine Lien Barkenæs Eggen, BCs., fysioterapeut. Forsterket rehabilitering Aker, Helseetaten, Oslo kommune. Tenesteleiar helse og velferd, Lom kommune. tonje.b.eggen@lom.kommune.no.
Anne Therese Tveter, PhD., fysioterapeut. Førsteamanuensis, Institutt for fysioterapi, Fakultet for helsevitenskap, OsloMet - storbyuniversitetet. Seniorforsker, Nasjonal kompetansetjeneste for revmatologisk rehabilitering, Klinikk for revmatologi og forskning, Diakonhjemmet sykehus.
Hege Ihle-Hansen, PhD., seksjonsoverlege, Oslo universitetssykehus HF, Nevrologisk avdeling, seksjon for hjerneslag.
Ingvild Hurum Rosseland, Executive master of management, fysioterapeut. Avdelingsleder, Forsterket rehabilitering Aker, Helseetaten, Oslo kommune.
Elisabeth Bø, PhD., spesialfysioterapeut og fagkoordinator, Oslo universitetssykehus HF.
Therese Brovold, PhD., fysioterapeut. Førsteamanuensis, Institutt for fysioterapi, Fakultet for helsevitenskap, OsloMet - storbyuniversitetet.
Denne vitenskapelige artikkelen er fagfellevurdert etter Fysioterapeutens retningslinjer, og ble akseptert 20.desember 2021. Studien er godkjent av personvernombudet ved Oslo universitetssykehus. Ingen interessekonflikter oppgitt.
Sammendrag
Hensikt: Akutt hjerneslag kan bidra til redusert selvstendighet og aktivitetsbegrensninger i dagliglivet. Hensikten med denne studien var: 1) å identifisere hvilke aktiviteter pasienter med akutt hjerneslag hadde problemer med å utføre målt med Pasientspesifikk funksjonsskala (PSFS), 2) å undersøke endring i PSFS og 3) å identifisere ulike faktorer assosiert med endringen etter 6 måneder.
Design/metode: Prospektivt kohortstudie hvor PSFS ble brukt som utfallsmål ved baseline, etter 4 uker og 6 måneder. Alle aktivitetene ble klassifisert med ICF. Kognitiv funksjon ble målt med Montreal Cognitive Assessment (MoCA).
Materiale: Studien inkluderte 61 deltakere rekruttert mens de var innlagt på en akutt slagenhet. Gjennomsnittsalder: 73 år. Seksti-sju prosent av studiedeltakerne var menn.
Resultat: Deltakerne oppga 150 aktiviteter som ble klassifisert under ICF domene mobilitet (d4), hjemmeliv (d6) og samfunns- og sosiale livsområder (d9). Det var en statistisk signifikant endring i PSFS skår mellom baseline, 4 uker og 6 måneder. MoCA ved baseline hadde størst sammenheng med endringen i PSFS.
Konklusjon: Deltakerne klarte å fylle ut PSFS og å skåre sine aktivitetsbegrensninger. Det var stor variasjon i oppgitte aktiviteter, noe som indikerer at pasientspesifikke standardiserte måleverktøy bør inkluderes i et testbatteri for pasienter med akutt hjerneslag. Deltakerne hadde en betydelig endring i selvrapporterte aktiviteter, der kognitiv funksjon hadde størst sammenheng med endringen i PSFS.
Nøkkelord: PSFS, hjerneslag, aktivitetsbegrensninger, ICF.
Abstract
Patient- Specific Functional Scale among people with acute Stroke in Norway
Purpose: Acute stroke can lead to reduced independence and activity restrictions in daily life. The aims of this study were: 1) to identify which self-reported activities stroke patients had difficulty to perform using the Patient- Specific Functional Scale (PSFS). 2) To evaluate change in PSFS and 3) to investigate different factors associated with change from baseline to 6 months.
Design/method: A prospective cohort design where PSFS was used as an outcome measure at baseline, after 4 weeks and 6 months. All activities were classified with ICF. Cognitive function was assessed with Montreal Cognitive Assessment (MoCA).
Material: Sixty-one participants, 67 % men, mean age 73 years, were included while admitted to an acute stroke unit.
Results: The participants reported 150 activities in PSFS that were classified under the domain mobility (d4), home life (d6) and society and social life areas (d9). There was a statistically significant change on PSFS score from baseline to 6 months. MoCA at baseline was associated with change in PSFS.
Conclusion: The participants managed to fill out PFSF and score their difficulty. There was a wide range of activity problems among the participants which suggest that it is important to include patient specific outcome measures for patients with stroke. The participants showed a meaningful change in self-reported activities, and cognitive function was strongest associated with the change in PSFS.
Keywords: PSFS, stroke, activity restrictions, ICF.
Innledning
Hjerneslag er en av de viktigste årsakene til langvarige funksjonsnedsettelser og redusert selvstendighet i dagliglivets aktiviteter (ADL). Mellom 50–70 % av pasientene som rammes er i behov av langvarig rehabilitering (1). Bedring av fysisk funksjon og økt selvstendighet i ADL er målet med rehabiliteringen, og for å sette mål og evaluere effekter og endringer er det anbefalt å bruke standardiserte måleverktøy. Tradisjonelle måleverktøy for kartlegging av funksjon etter et hjerneslag er Barthel ADL-Index (BI), Modified Rankin Scale (mRS) og prestasjonsbaserte funksjonsmål som ganghastighet og balanse (2). Dette er kliniker-rapporterte utfallsmål, hvor data samles inn ved at helsepersonell observerer og vurderer pasientens funksjon basert på en standardisert manual (3). Det anbefales også å inkludere pasientrapporterte utfallsmål ((Patient Reported Outcome Measures (PROM)) for å kartlegge pasientens egen opplevelse av funksjonsvansker, ofte gjennom strukturerte spørreskjema med predefinerte spørsmål (1-2,4). Pasientspesifikke måleinstrumenter er en underkategori av PROM som skiller seg fra kliniker-rapporterte måleinstrumenter og strukturerte spørreskjema ved at pasienten selv definerer hvilke aktiviteter og domener som måles (4,5). Pasientspesifikk funksjonsskala (PSFS) (6,7) benyttes i nettverket «Gode pasientforløp», og Folkehelseinstituttet (FHI) anbefaler det benyttet som grunnlag for tildeling av tjenester til pasienter (8,9). PSFS ble utviklet for pasienter med muskelskjelettplager, men kan også anvendes for å identifisere aktivitetsbegrensninger hos personer med nevrologiske lidelser som ervervet hjerneskade (10) og Parkinsons sykdom (11). Så vidt vi vet er det ingen tidligere studier som har undersøkt hvilke aktiviteter pasientene oppgir etter et akutt hjerneslag og hvilke endringer som skjer i selvrapporterte aktiviteter.
Hensikten med denne studien var derfor å kartlegge og klassifisere hvilke selvrapporterte aktiviteter, målt med PSFS, pasienter med akutt hjerneslag har problemer med å utføre på grunn av det aktuelle hjerneslaget. I tillegg ønsket vi å undersøke endring i PSFS fra innleggelse (baseline) til 4 uker og 6 måneder etter utskrivelse og identifisere ulike faktorer assosiert med endringen.
Materiale og metode
Design
Studien hadde et prospektivt kohort-design, og inkluderte pasienter med akutt hjerneslag innlagt ved Seksjon for hjerneslag, Oslo Universitetssykehus (OUS), og fulgte pasientene fra utskrivelse og 6 måneder frem i tid. Studien ble gjennomført i samarbeid mellom OUS, Helseetaten og OsloMet i perioden 2017-2019. Studien ble støttet av Fylkesmannen i Oslo og Viken, og ble vurdert av Regional etisk komite (REK) som en kvalitetsikringsstudie og dermed ikke fremleggingspliktig. Personvernombudet ved OUS har godkjent studien. Aktuelle deltakere ga skriftlig samtykke til deltakelse.
Utvalg
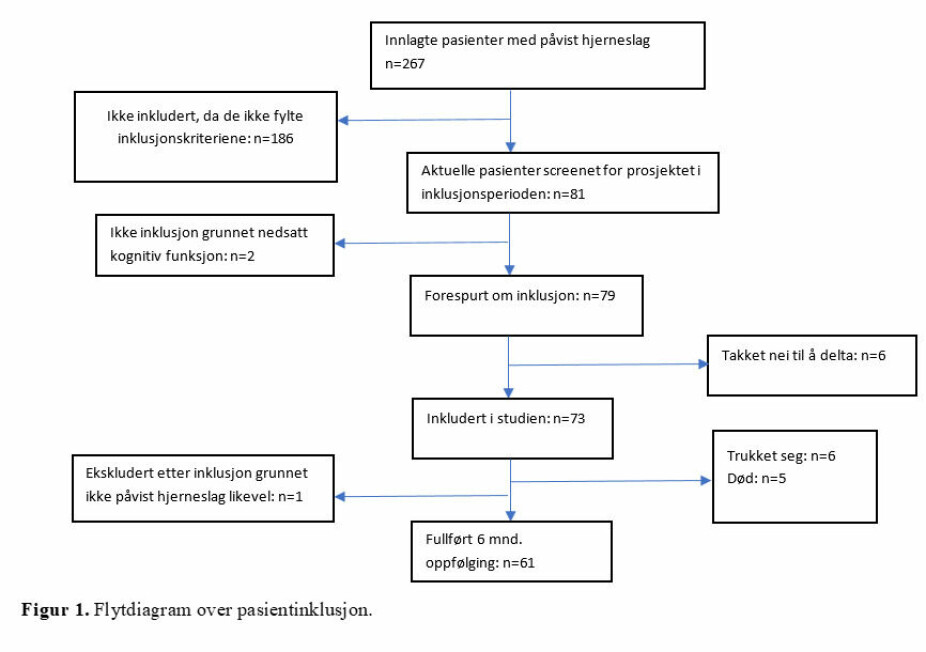
Pasienter ble rekruttert i perioden 01.05.18 til 31.10.18, en periode med totalt 267 innleggelser av pasienter med hjerneslag. Pasienter over 18 år med påvist akutt hjerneinfarkt eller hjerneblødning ble inkludert. Deltakerne skulle i tillegg være hjemmeboende før det aktuelle hjerneslaget, ikke ha kjent kognitiv svikt før hjerneslaget og være vurdert av personalet til å ha behov for videre rehabilitering etter utskrivelse. Pasienter som kun hadde behov for oppfølging av logoped grunnet dysfagi eller afasi, men ikke hadde andre fysiske eller kognitive funksjonsnedsettelser, ble ekskludert fra studien. Ekskludert ble også de som ikke ble vurdert til å ha et rehabiliteringspotensiale. Totalt 73 deltakere ble initiert inkludert, men en ble senere ekskludert da vedkommende likevel ikke hadde hatt et hjerneslag. Av disse fullførte 61 deltagere 6-månedersoppfølgingen, og ble dermed inkludert i analysen (Figur 1). All kartlegging ble gjennomført av de ansatte ved slagseksjonen og to prosjektmedarbeidere.
Datainnsamling
Demografiske data som kjønn, alder, type slag (hjerneinfakt/hjerneblødning) og slagets alvorlighetsgrad, målt ved The National Institutes of Health Stroke Scale (NIHSS) ved inklusjon, ble hentet fra pasientjournal, mens informasjon om sivilstatus, røyking, arbeidsstatus og utdanningsnivå ble samlet inn direkte fra deltakerne. Fysisk funksjon ved baseline ble målt og kategorisert med BI og mRS, og testet med Short Physical Performance Battery (SPPB) inkludert ganghastighet. Kognitiv funksjon ved baseline ble testet med Montreal Cognitive Assessment Scale (MoCA). Utskrivelsesdestinasjon og oppholdssted ved 4 uker og 6 måneder ble registrert.
Måleinstrument
Deltakerne fylte ut PSFS ved baseline og ved kontroll etter 4 uker og 6 måneder. Baseline-testingen ble gjennomført i slagseksjonen, ved kontroll der pasienten var på det aktuelle tidspunktet.
Pasientspesifikk funksjonsskala (PSFS)
PSFS ble utviklet av Stratford med kollegaer i 1995 med mål om å identifisere aktivitetsbegrensninger og er validert og reliabilitetstestet blant pasienter med ulike muskel- og skjelettplager og hos eldre (6, 12). Den norske versjonen er reliabilitetstestet for pasienter med muskel- og skjelettplager, men kun første aktivitet oppnådde akseptabel reliabilitet (ICC 0.83) (7). Minste målbare endring (Minimal Detectable Change, MDC) representerer den minste endringen man kan betrakte som reell endring (13). For PSFS, med et konfidensintervall (KI) 90 %, ble minste målbare endring estimert til 2.1 poeng (7).
Deltakerne fylte ut PSFS selvstendig, men de som hadde behov for hjelp fikk assistanse til å skrive. Deltakerne ble bedt om å rapportere sine aktivitetsbegrensninger i PSFS ved å beskrive inntil tre viktige aktiviteter, oppgitt som aktivitet 1, 2 og 3, som de hadde vansker med å utføre eller ikke kunne utføre i det hele tatt som følge av det aktuelle hjerneslaget. Deretter ble deltakerne bedt om å gradere vanskeligheten på en skala fra 0-10 hvor 0 representerer ingen vansker og 10 at aktiviteten ikke kan gjennomføres. Ved andre- og tredjegangs utfylling av PSFS ble deltakerne bedt om å skåre vanskelighetsgrad på de samme aktivitetene på nytt.
Klassifisering av PSFS i henhold til ICF
Aktivitetene deltakerne oppga på PSFS ble klassifisert i henhold til «Internasjonal klassifikasjon av funksjon, funksjonshemming og helse» (ICF) (gjennomført av T.L.B.E og T.B der uenighet ble diskutert til konsensus ble oppnådd). ICF er et rammeverk utviklet av Verdens Helseorganisasjon, for å klassifisere funksjon og funksjonshemming etter sykdom og skade (14). Aktivitetene ble klassifisert ved å velge domene (f.eks. d3 kommunikasjon), kategori (f.eks. kommunikasjon-ytre seg) og sub-domene (d330, tale).
Statistiske analyser
Statistikkprogrammet IBM SPSS versjon 26 ble benyttet for analyse av data. Kategoriske data ble beskrevet med absolutt (n) og relativ frekvens (%), mens kontinuerlige variabler ble beskrevet med gjennomsnitt og standardavvik (SD) hvis normalfordelte data og median, 25 og 75 kvartiler hvis ikke-normalfordelte data. Det ble regnet ut en endringsskår fra baseline til 6 måneder for PFSF aktivitet 1, 2 og 3. Endring over tid for PSFS aktivitet 1,2 og 3 ble analysert med repeterte målinger General Linear Model, hvor effekt av tid ble brukt som repetert målingsfaktor for utfallsmålene ved baseline, 4 uker og 6 måneder.
Univariate analyser ble gjennomført for å undersøke sammenheng mellom endring i PSFS aktivitet 1 og mulige forklaringsvariabler. Disse variablene ble valgt ut på bakgrunn av tidligere forskning og klinisk erfaring. Variabler med en p-verdi < 0.2 i de univariate analysene ble inkludert i den multiple regresjonsanalysen. Standard multippel regresjonsanalyse ble brukt for å undersøke hvilke av de uavhengige variablene (NIHSS, mRS, type slag, kognitiv og fysisk funksjon; BI, SPPB og ganghastighet) som hadde sammenheng med avhengig variabel (endring i PSFS fra baseline til 6 måneder).
Der hvor uavhengige variabler hadde en samvariasjon (Pearsons R) > 0.7, ble variabelen med størst faglig interesse, valgt ut. Alder og kjønn ble vurdert som mulige konfunderende faktorer, og ble inkludert i den endelige modellen.
Resultater
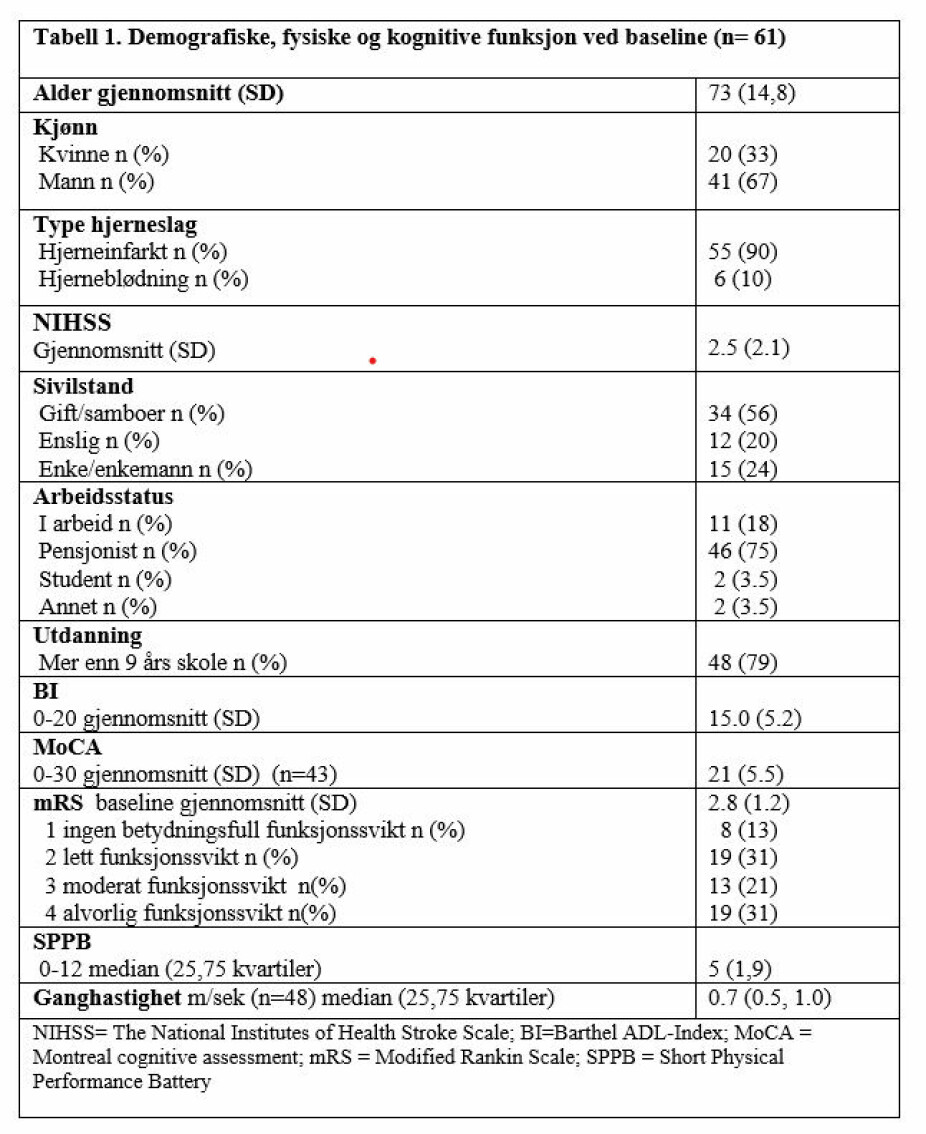
Deltagernes karakteristika, og fysiske og kognitive funksjon ved baseline, er presentert i tabell 1. Gjennomsnittlig alder var 73 (SD 14.8) år der fire deltagere var under 50 år, og 32 (54 %) var over 75 år. Av studiedeltakerne var 67 % menn og 90 % hadde hatt et hjerneinfarkt. MoCA ble testet hos 43/61 deltagere under oppholdet med gjennomsnittskår på 21 (SD 5.5). 32 (53 %) av deltakerne hadde moderat eller alvorlig funksjonssvikt (mRS 3-4). Deltakerne som ikke fullførte 6 måneders oppfølgingen (n=11) skilte seg ikke statistisk signifikant fra deltakerne som fullførte, hverken på alder eller NIHSS ved baseline.
Etter fire uker ble 34 (56 %) av deltakerne testet hjemme mens 20 (33 %) fremdeles var på rehabiliteringsopphold. Etter 6 måneder ble 56 (92 %) av deltakerne testet hjemme.
Aktivitetsbegrensninger målt med PSFS
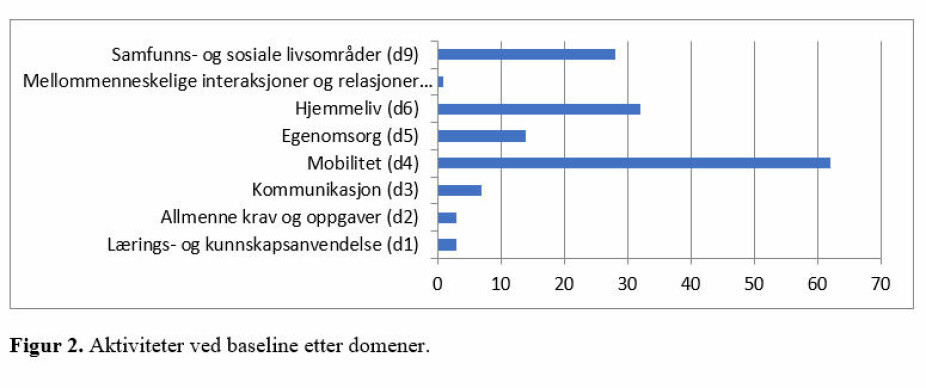
Totalt 58 av 61 deltakere fylte ut PFSF mens de var innlagt på slagseksjonen. Deltakerne oppgav til sammen 150 aktiviteter på PSFS. Tre deltakere klarte ikke å komme på noen aktivitet de hadde vansker med å utføre mens de var innlagt, men ved oppfølging etter fire uker og 6 måneder oppga de aktiviteter de hadde vansker med å utføre og skåret i PSFS. Disse aktivitetene ble inkludert i analysen. Deltakerne fikk selv velge fritt i aktiviteter, og de varierte fra enkeltstående oppgaver som «å sykle» og «å komme ut av sengen» til sammensatte oppgaver som å «rydde garasjen» og «å reise til England». Alle aktivitetene kunne klassifiseres ved å benytte ICF. De fleste aktivitetsbegrensningene ble klassifisert under domenene mobilitet (d4) (41 %), hjemmeliv (d6) (21 %) og samfunns- og sosiale livsområder (d9) (19 %).
Endring i aktivitetsbegrensninger
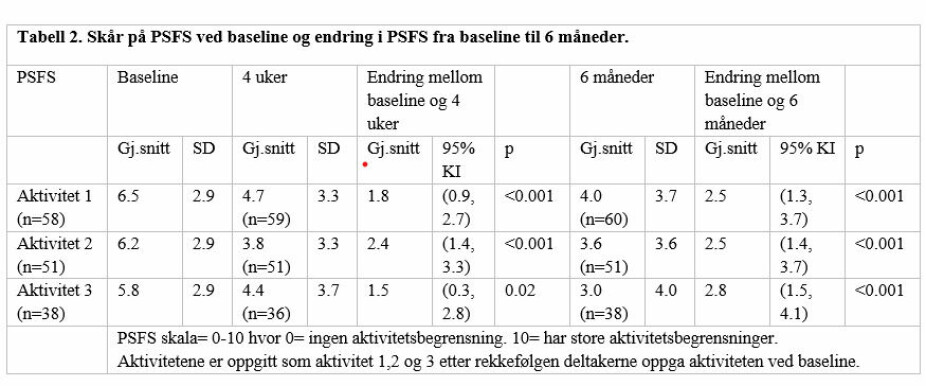
Tabell 2 viser at det var en statistisk signifikant endring i PSFS skår fra baseline til 6 måneder for alle tre aktivitetene. Pasientene oppga størst aktivitetsbegrensning knyttet til aktivitet 1 og 2 på PSFS.
Tretti-fire (55 %) deltakere i denne studien oppnådde minste kliniske relevante endring for den første aktiviteten på PSFS fra baseline til 6 måneder.
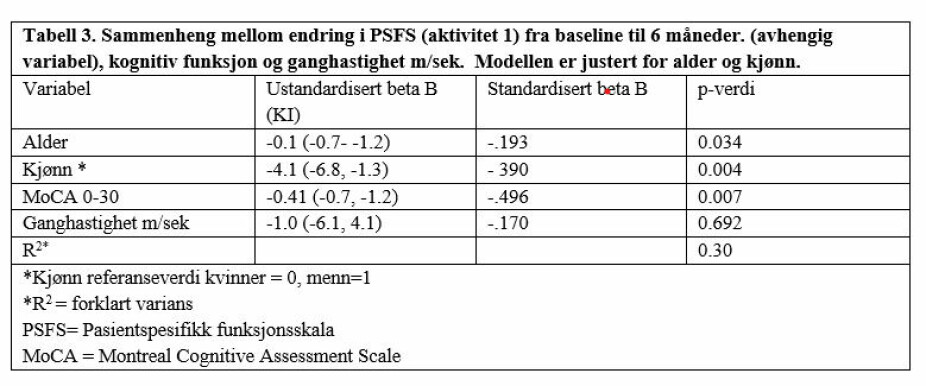
Kognitiv funksjon (målt ved MoCA), og ganghastighet var signifikant korrelert med endring i PSFS fra baseline til 6 måneder, og ble inkludert i den multiple regresjonsmodellen. NIHSS, mRS, type slag, SPPB ved baseline hadde ingen sammenheng med avhengig variabel (p >0.2), og ble ikke inkludert. Resultatene fra den multiple regresjonsmodellen er vist i tabell 3, og viser at 1 poeng høyere skår på MoCA var assosiert med -0.41 poeng mindre endring på PSFS. Modellen er justert for alder og kjønn.
Diskusjon
Hensikten med denne studien var å kartlegge og klassifisere hvilke selvrapporterte aktiviteter, målt med PSFS, pasienter med akutt hjerneslag har problemer med å utføre på grunn av hjerneslaget. Vi ønsket også å undersøke endring i PSFS fra innleggelse til 4 uker og 6 måneder etter utskrivelse og identifisere ulike faktorer assosiert med endringen.
Målsetting er essensielt innen rehabilitering (15), og det anbefales pasientsentrerte mål (10). Studier beskriver at pasientens egne ønsker når det kommer til funksjonsforbedring bør vektlegges mer enn det gjør i dag (16). Ved å benytte PSFS som utfallsmål får pasienten selv definere aktiviteten som evalueres, hvilket sikrer at områder pasienten selv er opptatt av kan identifiseres og evalueres som ledd i rehabiliteringsprosessen. Dette kan være en styrke sammenlignet med generiske spørreskjema, som ikke nødvendigvis er sensitive nok for den enkelte pasient som besvarer skjemaet (17). Denne variasjonen i oppgitte aktiviteter har blitt diskutert som en begrensing for å måle endring (5), hvor både det å "gå en tur i hagen" og "å reise til England" tallfestes med samme tallverdi i PSFS. Tidligere studier viser derimot at PSFS kan være egnet for å involvere pasienter i utarbeidelse av mål og prioriteringer, og på denne måten bidra til økt samvalg, samt registrere endring i de aktivitetene pasienten selv oppgir som utfordrende gjennom behandlingsforløpet (7,10).
Våre resultater viser at deltakerne, som hadde varierende nivå av fysisk og kognitiv funksjon, klarte å fylle ut PSFS og skåre sine vansker mens de var innlagt på sykehuset. Noen av deltakerne opplevde en aktivitetsbegrensning med grunnleggende, basale aktiviteter, mens andre deltakere opplevde aktivitetsbegrensninger som handler om aktiviteter som ikke nødvendigvis er viktige for å kunne klare seg hjemme, men som er viktige for å delta i samfunnet og kunne være med på fritidsaktiviteter. Mange av aktivitetene pasientene i denne studien oppga er ikke med i de mest vanlige måleinstrumentene som brukes for pasienter med hjerneslag (2). Dette kan tyde på at å leve et selvstendig liv for mange innebærer å mestre daglige aktiviteter som å kunne kle på seg selv og å kunne gå, men også mer komplekse, sammensatte aktiviteter som å kjøre bil og bedrive fritidsaktiviteter.
Seks måneder etter hjerneslaget viste PSFS aktivitet 1 en median skår på 4, noe som tyder på at mange av deltakerne fortsatt opplevde aktivitetsbegrensninger på den første aktiviteten de nevnte. Studier som har sett på dette for pasienter mer enn 1 år etter hjerneslaget viser at pasienter med hjerneslag ofte opplever aktivitetsbegrensninger innen områdene ADL, mobilitet og fritidsaktiviteter (18,19). Dette tyder på at det kan være viktig å inkludere pasientspesifikke måleinstrumenter for å identifisere hvilke aktiviteter pasientene opplever begrensninger i etter et hjerneslag. Resultatene viser at alle deltakerne fikk en signifikant endring i selvrapportert aktivitet 1 og 2 på PSFS. Gjennomsnittlig endring var 2.5 poeng for både aktivitet 1 og 2, noe som er over minste målbare endring vist i liknende studier (7,10).
I denne studien undersøkte vi også hvilke variabler som hadde sammenheng med endring i PSFS skår fra baseline til 6 måneder, der MoCA var den variabelen som kunne forklare mest av variasjonen i endringen. En mulig tolkning av dette resultatet er at deltagere med redusert kognitiv funksjon viste mindre progresjon målt med PSFS enn andre deltakere med høyere skår på MoCA. Dette resultatet samsvarer med studien til Evensen med flere (2020), som også fant en sterk sammenheng mellom endring i PSFS og kognitiv funksjon hos deltakere som var på rehabilitering etter en ervervet hjerneskade. En annen likhet med denne studien var at personer med redusert kognitiv funksjon klarte å fylle ut PSFS og skåre sine aktivitetsbegrensninger. Så vidt vi vet er dette den første studien i Norge som har inkludert PSFS for å måle aktivitetsbegrensninger etter akutt hjerneslag. Det er gjort få eller ingen studier som har evaluert PSFS i en tidlig fase etter hjerneslag. Konsekvensen av dette er at testens psykometriske egenskaper ved akutt slag ikke er kjent, noe som gjør at vi tolker resultatene med større forsiktighet.
Fremtidige studier bør undersøke videre hvordan PSFS best kan brukes hos pasienter med redusert kognitiv funksjon etter akutt hjerneslag.
Styrker og svakheter ved studien
En styrke ved denne studien er dens prospektive design og at alle pasienter med hjerneslag innlagt ved OUS i perioden 1.5.-31.10.18, som hadde behov for rehabilitering ble inkludert. Det er også en styrke at studien inkluderte deltakere med redusert kognitiv funksjon. En svakhet er at kriteriene for å vurdere hvem som hadde behov for rehabilitering ikke ble fastsatt på forhånd (20). Vi kjenner derfor ikke til hva som kjennetegner deltagere som ikke oppfylte disse kriteriene og som ble ekskludert, noe som kan påvirke generaliserbarheten. Deltakerne som ble inkludert i studien hadde en median NIHSS på 2 og mRS på 2.8 ved baseline, som igjen indikerer at de dårligste pasientene ikke er representert i denne studien. Oppfølgingstid er avgjørende i en kohort studie. I denne studien ble deltakerne fulgt i 6 måneder. Dette kan være for kort tid etter et hjerneslag. Imidlertid kan lang oppfølgingstid øke risikoen for frafall. En styrke ved denne studien er lavt frafall (15%) og at det ikke var noen forskjell i alder eller skår på NIHSS mellom deltagere som fullførte og de som falt fra. En svakhet er at PSFS ikke er validitets- og reliabilitetstestet hos personer med akutt hjerneslag.
Konklusjon
Resultatene fra studien bidrar med nyttig kunnskap om hvilke aktiviteter pasientene selv opplever at de har vansker med å gjennomføre etter akutt hjerneslag. De fleste aktivitetsbegrensningene ble klassifisert under domenene mobilitet, hjemmeliv og samfunns- og sosiale livsområder. Det var stor variasjon i oppgitte aktiviteter. Deltakerne hadde en betydningsfull endring i selvrapporterte aktiviteter. Kognitiv funksjon hadde størst sammenheng med endring på PSFS. Det anbefales flere studier for å undersøke bruk av PSFS i målsetting etter hjerneslag og om målene endrer seg gjennom et rehabiliteringsforløp.
Takk til Forsterket Rehabilitering Aker for muligheten til å gjennomføre prosjektet. Takk til fysioterapeut M.Sc. Åse Bergheim, vår kollega i prosjektet, og til fysioterapeutene ved slagenheten OUS for godt samarbeid og bidrag inn i studien.
Litteraturliste
1. Helsedirektoratet: https://www.helsedirektoratet.no/tema/hjerneslag
2. Moore JL, Potter K, Blankshain K. et al. A Core Set of Outcome Measures for Adults With Neurologic Conditions Undergoing Rehabilitation: A CLINICAL PRACTICE GUIDELINE. J Neurol Phys Ther. 2018 Jul;42(3):174-220. https:/www.doi.org/10.1097/NPT.0000000000000229.
3. Reeves M, Lisabeth L, Williams L. et al. Patient-Reported Outcome Measures (PROMs) for Acute Stroke: Rationale, Methods and Future Directions. Stroke. 2018 Jun;49(6):1549-1556. https:/www.doi.org/10.1161/STROKEAHA.117.018912.
4. Horn KK, Jennings S, Richardson G. et al. The patient-specific functional scale: psychometrics, clinimetrics, and application as a clinical outcome measure. J Orthop Sports Phys Ther. 2012 Jan;42(1):30-42. https:/www.doi.org/10.2519/jospt.2012.3727.
5. Nicholas P, Hefford C, Tumilty S. The use of the Patient-Specific Functional Scale to measure rehabilitative progress in a physiotherapy setting. J Man Manip Ther. 2012 Aug;20(3):147-52. https:/www.doi.org/10.1179/2042618612Y.0000000006.
6. Stratford P, Gill C, Westaway M. et al. (1995). Assessing disability and change on individual patients: a report of a patient specific measure. Physiotherapy canada, 47(4), 258-263.
7. Moseng T, Tveter AT, Holm I. et al. (2013). Pasient-Spesifikk Funksjons Skala: Et nyttig verktøy for fysioterapeuter i primærhelsetjenesten. Fysioterapeuten, 2, 20-26.
8. Folkehelseinstituttet: https://www.fhi.no/publ/skjema/hva-er-viktig-for-deg---skjema-pasientspesifikk-funksjonsskala---psfs/
9. Helsenorge: www.helsenorge.no/samvalg-v2/hva-er-samvalg/
10. Evensen J, Soberg HL, Sveen U, Hestad KA, Bronken BA. The Applicability of the Patient-Specific Functional Scale (PSFS) in Rehabilitation for Patients with Acquired Brain Injury (ABI) - A Cohort Study. J Multidiscip Healthc. 2020 Oct 9;13:1121-1132. https:/www.doi.org/10.2147/JMDH.S259151.
11. Bohannon RW, Nair P, Green M. Feasibility and informativeness of the Patient-Specific Functional Scale with patients with Parkinson's disease. Physiother Theory Pract. 2020 Nov;36(11):1241-1244. https:/www.doi.org/10.1080/09593985.2019.1571134.
12. Mathis RA, Taylor JD, Odom BH, Lairamore C. Reliability and Validity of the Patient-Specific Functional Scale in Community-Dwelling Older Adults. J Geriatr Phys Ther. 2019 Jul/Sep;42(3):E67-E72. https:/www.doi.org/10.1519/JPT.0000000000000188.
13. Terwee CB, Bot SD, de Boer MR, van der Windt DA, Knol DL, Dekker J, Bouter LM, de Vet HC. Quality criteria were proposed for measurement properties of health status questionnaires. J Clin Epidemiol. 2007 Jan;60(1):34-42. https:/www.doi.org/10.1016/j.jclinepi.2006.03.012.
14. World Health Organization. (2006). Internasjonal klassifikasjon av funksjon, funksjonshemming og helse, ICF. KITH, redaktør. Oslo Sos Og Helsedirektoratet, 2, 222.
15. Levack WM, Weatherall M, Hay-Smith EJ, Dean SG, McPherson K, Siegert RJ. Goal setting and strategies to enhance goal pursuit for adults with acquired disability participating in rehabilitation. Cochrane Database Syst Rev. 2015 Jul 20;(7):CD009727. https:/www.doi.org/10.1002/14651858.CD009727.
16. Gzil F, Lefeve C, Cammelli M, Pachoud B, Ravaud JF, Leplege A. Why is rehabilitation not yet fully person-centred and should it be more person-centred? Disabil Rehabil. 2007 Oct 30-Nov 15;29(20-21):1616-24. https:/www.doi.org/10.1080/09638280701618620.
17. Moseng, T. Pasientspesifikt funksjonsmål: Et verktøy til bruk i fysioterapipraksis? Masteroppgave. Oslo: Universitetet i Oslo, 2011.
18. Harris JE, Eng JJ. Goal Priorities Identified through Client-Centred Measurement in Individuals with Chronic Stroke. Physiother Can. 2004 Jun;56(3):171-176. https:/www.doi.org/10.2310/6640.2004.00017.
19. Hartman-Maeir A, Soroker N, Ring H, Avni N, Katz N. Activities, participation and satisfaction one-year post stroke. Disabil Rehabil. 2007 Apr 15;29(7):559-66. https:/www.doi.org/10.1080/09638280600924996.
© Author(s) (or their employer(s)) 2022. Re-use permitted under CC BY-NC. No commercial re-use. See rights and permissions (https://creativecommons.org/licenses/by-nc/4.0/). Published by Fysioterapeuten.























