Intradialytisk trening av kroniske nyrepasienter
Fagartikkel i Fysioterapeuten 10/2013.
Heidi Agnor Bunæs-Næss, spesialfysioterapeut, Cand Mag., Oslo universitetssykehus HF, Medisinsk klinikk, Seksjon for fysioterapi, Ullevål. uxbunh@ous-hf.no.
Aud-Eldrid Stenehjem, avdelingsoverlege, PhD, Oslo universitetssykehus HF, Medisinsk klinikk, Nyremedisinsk Avdeling, Ullevål.
Birgitta Blakstad Nilsson, seniorforsker, Oslo universitetssykehus HF, Medisinsk klinikk, seksjon for fysioterapi, og førsteamanuensis, Høgskolen i Bergen, Institutt for ergoterapi, fysioterapi og radiografi.
Fagartikkelen er fagfellevurdert etter Tidsskriftet Fysioterapeutens retningslinjer. Akseptert 7.8.2013. Ingen interessekonflikter oppgitt.
Sammendrag
Innledning: Pasienter med kronisk nyresykdom i hemodialyse (HD) utvikler komplikasjoner som påvirker tilnærmet alle organsystemene. Muskeltap og spesielt proksimal muskelsvakhet er vanlig hos pasienter med kronisk nyresykdom i stadium 5 (dialysestadiet). Pasientene har også betydelig lavere livskvalitet sammenlignet med aldersfriske. Flere studier har vist at hemodialysepasienter har mange effekter av trening, men det er få studier som har evaluert effekt av trening som gjennomføres samtidig som pasienten får hemodialysebehandling (intradialytisk trening). Hemodialyse gjøres på sykehus tre-fire timer, minst tre ganger per uke.
Hensikt: Hensikten med denne fagartikkelen er å redegjøre for kunnskap om trening av pasienter med kronisk nyresvikt i stadiet 5 og å belyse evidensbasert kunnskap om effekter på fysisk yteevne og livskvalitet på intradialytisk trening.
Hoveddel: Styrketrening eller en kombinasjon av styrke- og kondisjonstrening er de mest studerte intervensjonene. Treningsprogrammene er mangelfullt beskrevet og dermed vanskelig å sammenligne. Kondisjonstrening gjennomføres under hemodialysens påbegynte andre time, enten sittende på en ergometersykkel, eller halvt liggende i dialysestol i en spesialtilpasset sengesykkel. Styrketrening er hovedsakelig beskrevet som bruk av egen kroppsvekt eller ved bruk av theraband og ankelmansjetter.
Avslutning: Evidensgrunnlaget for intradialytisk trening av kroniske nyrepasienter er svakt. Det er etter vårt syn behov for større randomiserte studier som sammenligner forskjellige treningsmodaliteter før man kan anbefale den best egnede treningsform for kroniske nyrepasienter i HD. Fysioterapeuter har en viktig rolle med hensyn til tilrettelegging og trening av kronisk nyresyke og vil kunne spille en betydelig rolle i fremtidig behandling av dialysepasienter.
Nøkkelord: intradialytisk trening, fysisk trening, hemodialyse, kronisk nyresvikt.
Introduksjon
Kronisk nyresvikt er en stille alvorlig sykdom og fører til en gradvis forverring av nyrefunksjonen. Forekomsten er økende på verdensbasis (1-3), og i Norge er forekomst av kronisk nyresvikt i den generelle befolkning ti til elleve prosent (4). Hypertensjon er den viktigste årsaken til nyresvikt, etterfulgt av diabetes nefropati og glomerulonefritt (3).
Nyresykdom deles inn i fem stadier, basert på i hvilken grad nyrefunksjonen (glomerulær filtrasjonsrate = GFR) er redusert (4, 5) (tabell 1).

Aktiv uremibehandling i form av hemodialyse (HD), peritonealdialyse (PD) eller nyretransplantasjon (Tx) er nødvendig i stadium fem (GFR er omlag 5-10 ml/min) (4, 5).
Behandling av kronisk nyresyke består i å forsinke progresjon av nyreskaden, behandle grunnsykdom, samt å forebygge systemiske komplikasjoner (2, 5, 6) Dialysebehandling er krevende og tolereres dårligst av eldre og av personer med hjerte- og karsykdom (2, 5). Pasientene er tilkoblet dialysemaskinen tre til seks ganger per uke, tre til fire timer per gang i stillesittende posisjon (5, 7, 8).
Kronisk nyresyke med dialysebehov utvikler komplikasjoner som påvirker tilnærmet alle organsystemene (9). Muskelatrofi er beskrevet som en av de sterkeste prediktorer for mortalitet i denne pasientpopulasjonen (7). Pasientene har også halvert arbeidskapasitet sammenlignet med aldersfriske (10, 11). Til tross for medisinske fremskritt innen nyreerstattende behandling, er pasientenes funksjon, psykososiale status og helserelaterte livskvalitet betydelig redusert (11).
Det er god evidens for at kronisk nyresyke i predialysestadiene (stadium 1-4) forbedrer sin fysiske yteevne, muskelstyrke og livskvalitet med fysisk trening. Pasienter i PD, HD og nyretransplanterte har også vist forbedring og normalisering av fysisk form ved trening (5, 11). Til tross for dette er det, oss bekjent, ingen sykehus i Norge som tilbyr tilrettelagt trening for kroniske nyrepasienter som behandles med HD. De fleste studier har evaluert trening på dialysefrie dager. Nyere studier har vist at trening på dialysefri dag har dårlig compliance (7, 12). For å frigjøre pasientens tid utover dialysen til arbeid, sosialt liv eller hvile, er det interessant å evaluere hvilke effekter som kan oppnås ved intradialytisk trening.
Denne artikkelen er et resultat av litteratursøk i forbindelse med planlegging av en pilotstudie for å evaluere sengesykling med forskjellig intensitet hos HD pasienter på Oslo Universitetssykehus, Ullevål. Hensikten med artikkelen er å redegjøre for kunnskap om trening under HD og belyse evidensbasert kunnskap om effekter på fysisk yteevne og livskvalitet.
Årsaker til fysisk funksjonssvikt og symptomer
Nyrene har tre hovedfunksjoner: regulering av kroppsvæske og elektrolytter, utskillelse av avfallsstoffer og endokrin funksjon (produsere renin, erythropoietin, og å aktivere vitamin D) (2). Ved kronisk nyresykdom er pasientens hovedproblem betydelig redusert evne til å skille ut avfallsstoffer (6). Uremi er en katabol tilstand med mindre muligheter for kroppen til å kvitte seg med nedbrytningsprodukter (karbamid eller urinstoff) fra proteinomsetningen, som sammen med metabolsk acidose, fører til muskelnedbrytning og muskelatrofi (7, 13).
Nyrenes manglende evne til å produsere erythropoietin, som følge av et suksessivt nyrefunksjonstap gir renal anemi (14). Renal anemi og skjelettmuskel dysfunksjon er to av de viktigste årsakene til fysisk funksjonstap. Flere studier har vist korrelasjon mellom maksimalt oksygenopptak (VO 2max) og totalhemoglobinet (15,16).
Flere studier fremhever det alvorlige skjelettmuskeltapet hos HD pasientene (8, 10, 11), og årsakene er multifaktorielle: underernæring, medikamenter, komorbiditet, aldring/oksidativt stress, inaktivitet og acidose (2, 5, 7, 8, 11, 13, 14). Konsekvensene av dette muskeltapet innebærer fysiske-, psykologiske- og metabolske endringer (2, 5, 7, 8, 11). Psykologiske endringer kan medføre depresjon, angst, redusert vitalitet, redusert helserelatert livskvalitet, lav sosial funksjon og lav persepsjon av egen fysiske funksjon (5, 7, 8, 11, 17). De metabolske endringene kan medføre redusert perifer O2 ekstraksjon, reduksjon i muskelmasse og økt fettmasse, muskulær fatigue, redusert metabolsk funksjon og insulin resistens (7). De funksjonelle endringene kan være redusert arbeidskapasitet, vansker med dagliglivets aktiviteter, redusert deltakelse i fritidsaktiviteter og kronisk fatigue, (8-11).
Flere studier har vist at HD pasientene har en lavere oksidativ energimetabolisme i skjelettmuskulaturen sammenlignet med friske. Muskelfiberkomposisjonen kan ha en forskyvning mot fibre med et høyere oksidativt potensiale, type I- og II A fibre på bekostning av de anaerobe, type II B fibre (14).
Salt- og væskeretensjon samt påvirkning av renin-angiotensin systemet medfører utvikling av hypertensjon og økt forekomst av kardiovaskulære komplikasjoner (5). Problemer med regulering av kalsium-fosfat-vitamin D-parathyroidehormon-aksen leder til beinskjørhet og utvikling av forkalkninger. Samlet vil ubehandlet uremi gi uttalt trøtthet, søvnforstyrrelser, kløe, muskelkramper, muskelatrofi og etter hvert betydelig nedsatt fysisk yteevne (2, 5).
Hemodialyse
Under HD filtreres blodet og renses for avfallsprodukter, og overskuddsvæske trekkes ut i en dialysemaskin. HD over tid krever en god «blodåretilgang», helst i form av en arteriovenøs fistel, der arterien er direkte koblet til venen (2). Når venen er ferdig utviklet, plasseres to nåler i venen ved hver dialyse (5, 6). Alternativt benyttes sentralt venøst dialysekateter som legges i en tunnel under huden (2).
I noen tilfeller kan pasienten velge dialysemodalitet, mens det i andre tilfeller må vurderes ut fra den medisinske tilstanden. Det er stadig flere pasienter som behandles i dialyse uten at det er aktuelt med eller indikasjon for nyretransplantasjon (2, 5).
Median ventetid på nyre fra avdød giver er åtte til ti måneder, men for immuniserte pasienter kan ventetiden bli flere år (1). I Norge transplanteres 30 til 40 prosent med nyre fra levende giver (3).
Metode
Studien baserer seg på ikke-systematiske søk i PEDro, Cochrane Library og PubMed Clinical Queries, samt gjennomgang av referanselistene til relevante artikler. Førsteforfatter (HB-N) gjennomførte søkene og utvelgelsen av artiklene. Siste søk ble gjennomført i mai 2013. Studier fra og med 1995 ble vurdert.
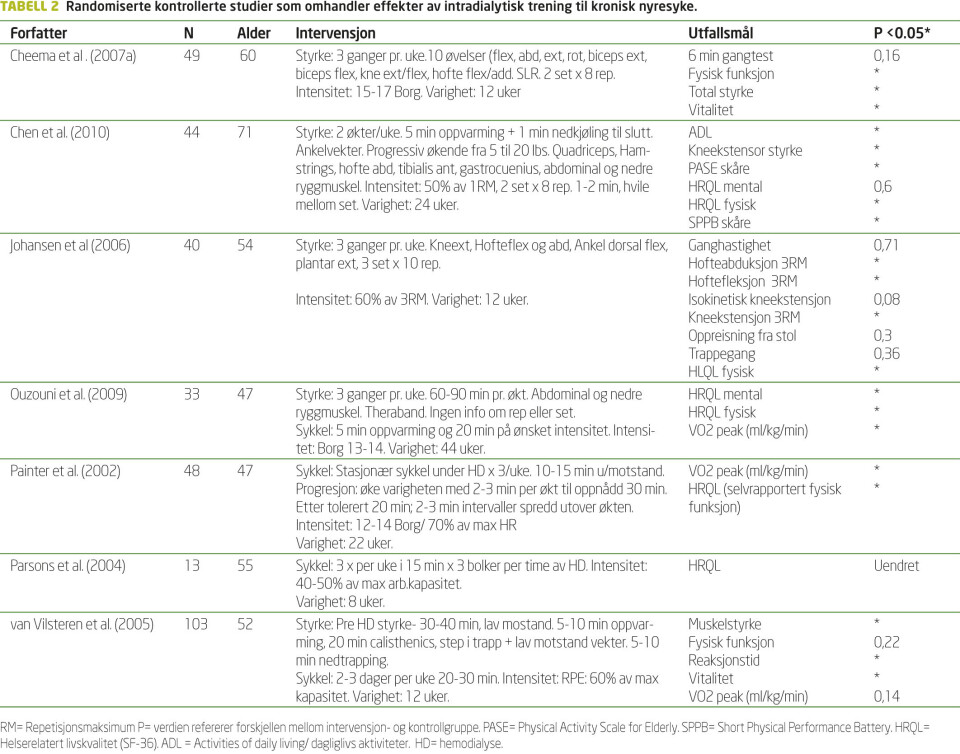
Det ble identifisert 26 studier som evaluerte effekt av utholdenhets - og eller styrketrening for HD pasienter. Nitten studier var randomiserte kontrollerte studier (RCT). Det kom tydelig frem i ti studier at intervensjonen var intradialytisk trening. I denne artikkelen presenteres og diskuteres syv utvalgte RCT-studier med fysisk yteevne og livskvalitet som hovedeffektmål (tabell 2). Primært diskuteres studier av moderat til god kvalitet. Studier med lav kvalitet i henhold til Cochrane´s Risk of Bias og PEDro skalaspørsmål er utelatt.
Hoveddel
Trening
Effekten av å trene kroniske nyresyke pasienter i HD er av klinisk betydning. De fysiske utfordringene pasientgruppen har er av interesse for fysioterapeuter som jobber med denne pasientgruppen – en pasientgruppe med økende insidens.
Kondisjonstrening
Painter og medarbeidere (18) randomiserte 48 HD pasienter (27 kvinner og 21 menn) til en kontrollgruppe og en treningsgruppe. Treningsgruppen trente kondisjonstrening med stasjonær sykkel under HD tre ganger per uke i 22 uker. Intensiteten i trening ble dosert med Borg skala (17) (12-14). VO2max og helserelatert livskvalitet økte signifikant i intervensjonsgruppene sammenlignet med kontrollgruppen (tabell 2).
Den andre studien som inkluderte kondisjonstrening (19) randomiserte 13 HD pasienter (6 kvinner og 7 menn) til en kontrollgruppe og en treningsgruppe. Treningsgruppen trente med stasjonær sykkel under HD tre ganger per uke i åtte uker. Intensiteten i trening ble dosert med en subjektiv skala, intensitet 40-50 prosent av maksimal arbeidskapasitet. VO2max ble målt under dialyse, uten at det er beskrevet hvordan. Det ble ikke funnet noen endring i helserelatert livskvalitet mellom gruppene (tabell 2).
Intervensjonens varighet var betydelig lenger i en studie (18), 22 uker versus åtte uker (19), noe som kan ha hatt betydning for resultatene i denne artikkelen. Intervensjonen i studien til Painter og medarbeidere (18) inkluderte intervaller på to til tre minutter, etter at 20 minutter kontinuerlig sykling ble tolerert. Det er ikke beskrevet hvor mange intervaller pasientene gjennomførte totalt. Parson og medarbeideres (19) intervensjon var stykket opp i bolker på tre perioder, hver med 15 minutters varighet og påbegynt i første, andre og tredje dialysetime. Treningsprotokollene viste at det var omtrent en tredjedel av pasientene som ikke fullførte siste 15 minutters bolk på grunn av hypotensjon. Hypotensjon er en vanlig komplikasjon i tredje og fjerde dialysetime. Det er videre økt risiko for kardiovaskulære komplikasjoner og kramper mot slutten av dialysetiden (19). Den relativt korte total intervensjonstiden sammen med korte økter kan ha påvirket resultatet.
Styrketrening
Cheema og medarbeidere (7) randomiserte 49 HD pasienter (15 kvinner og 34 menn) til en kontrollgruppe og treningsgruppe. Treningsgruppen trente styrkeøvelser for over- og underekstremiteter tre ganger pr. uke i 12 uker. Intensiteten i trening ble dosert med Borg skala (15-17). Kneekstensjon, total styrke og helserelatert livskvalitet økte signifikant i treningsgruppen sammenlignet med kontrollgruppen (tabell 2).
Chen og medarbeidere (20) randomiserte 44 HD pasienter (21 kvinner og 23 menn) til en kontrollgruppe og en treningsgruppe. Treningsgruppen trente styrke med ankelmansjetter og egen kropp som motstand i 24 uker. Intensiteten i trening ble dosert med en subjektiv skala med et mål om moderat intensitet på seks (noe hardt) av ti (ekstremt hardt), ekvivalent til 60 prosent av 1RM. Kneekstensjon økte signifikant i treningsgruppen sammenlignet med kontrollgruppen, samt en signifikant bedring i helserelatert livskvalitet.
Johansen og medarbeidere (8) randomiserte 40 HD pasienter (14 kvinner og 26 menn) til en kontrollgruppe og treningsgruppe. Treningsgruppen trente styrke av underekstremitetene i 12 uker. Intensiteten i styrketreningen var dosert med en subjektiv skala med et mål ekvivalent til 60 prosent av tre repetisjons maksimum (RM) i serier på 10 repetisjoner. Kneekstensjon økte signifikant i treningsgruppen sammenlignet med kontrollgruppen. Videre fikk intervensjonsgruppen en signifikant bedring i total muskelstyrke og helserelatert livskvalitet sammenlignet med kontrollgruppen (tabell 2).
Pasientenes egne opplevelser er også av betydning, og resultatene i to av studiene viste bedring i komponenten fysisk funksjon i SF 36 (8, 21), som er pasientens selvrapporterte opplevelse i forhold til egen fysisk funksjon.
Samtlige studier som har hatt styrketrening alene som intervensjon, har vist signifikant bedre muskelstyrke i intervensjonsgruppen. Chen og medarbeideres (20) intervensjon var styrketrening med relativt lav intensitet av lang varighet (seks måneder). Lengden på intervensjonen kan ha hatt betydning for disse resultatene ved at muskulaturen har fått tid til å få reell effekt av treningen, og at det ikke bare er en styrkeadaptasjon drevet av restrukturering av det nevromuskulære system (21). På den annen side kan det tenkes at populasjonen i denne studien i utgangspunktet var sykere enn den i de andre studiene, slik at en lavintensitets styrketrening gjorde større utslag på funksjon. Demografiske data lar seg vanskelig sammenligne, med unntak av alder, hvor Chen og medarbeidere (20) hadde en høyere snittalder på både intervensjons- og kontrollgruppen enn de øvrige studiene. Intervensjonsgruppen i denne studien hadde i tillegg en trend til flere år i HD (p=0.08) sammenlignet med kontrollgruppen. Selv om forskjellen ikke var signifikant, er det tenkelig at det kan ha påvirket resultatene.
Kombinasjon av styrke- og kondisjonstrening
Ouzouni og medarbeidere (11) randomiserte 33 HD pasienter (6 kvinner og 27 menn) til en kontrollgruppe og en treningsgruppe. Treningsgruppen trente styrke med theraband for underekstremiteter og abdominalmuskler, og kondisjonstrening med stasjonær sykkel i 44 uker. Intensiteten i trening ble dosert med Borg skala (13-14). Direkte måling av VO2max var hovedeffektvariabelen i denne studien.
VO2max økte signifikant i treningsgruppen sammenlignet med kontrollgruppen, og intervensjonsgruppen fikk en signifikant bedring i helserelatert livskvalitet i fysisk-, (men ikke i mental) komponent.
van Vilsteren og medarbeidere (10) randomiserte 103 HD pasienter (35 kvinner og 68 menn) til en kontrollgruppe og en treningsgruppe. Treningsgruppen trente styrke av underekstremitetene, abdominalmuskler og nedre ryggmuskler, samt kondisjonstrening med stasjonær sykkel i 12 uker. Intensiteten i trening ble dosert med en subjektiv skala ekvivalent til 60 prosent av maksimal kapasitet. VO2max ble målt indirekte i denne studien.
Total muskelstyrke økte signifikant i treningsgruppen sammenlignet med kontrollgruppen. Det var også en signifikant bedring i helserelatert livskvalitet; generell helsepersepsjon, vitalitet og helseendring (tabell 2).
Intervensjonen varte betydelig lenger i studien med signifikant økning i VO2max (11) (ti måneder), sammenlignet med den andre studien (10). Optimalt sett bør flere studier ligge til grunn, helst fra studier vurdert til å være av høy metodisk kvalitet, for å belyse effekten av en kombinasjon av styrke- og utholdenhetstrening under HD. Det er likevel av klinisk interesse at intervensjonsgruppen til Ouzouni og medarbeidere (11) trente på moderat intensitet (13-14 på Borg skala), og til tross for dette fikk en klinisk betydningsfull bedring av VO2max (4.4 ml/kg/min).
Risiko ved trening av pasienter i hemodialyse
Oss bekjent finnes det ingen studier som har evaluert risiko ved trening for hemodialysepasienter. Tilgjengelig kunnskap om risiko kommer fra studier som har rapportert om hendelser i effektstudier av trening (13). Det er mulig at kronisk nyresyke har en høyere risiko for muskelskjelettskader som et resultat av hyperparatyreoidisme og skjelettsykdommer. Dialysepasienter har økt risiko for benbrudd, hele 440 prosent høyere risiko for hoftebrudd enn den generelle befolkningen (22, 23). Det er også en større risiko for spontane senerupturer og senebetennelser for pasientgruppen (13). Når man skal tilrettelegge trening for pasienter i HD, kan det være hensiktsmessig med en god oppvarming på lav intensitet før intensitetsøkning, samt vektbærende øvelser for å forebygge skader. I den generelle befolkningen er muskelskjelettskader den vanligste risiko ved trening (13), de mest alvorlige risikoer er de med kardiovaskulært opphav, som arytmier, iskemi eller plutselig død (13). Skaderisikoen øker også med økt intensitet på treningen (13). Kronisk nyresyke har høyere prevalens av kardiovaskulære sykdommer enn den generelle befolkningen (13). Av den grunn synes det hensiktsmessig å arbeidsbelaste pasientene før oppstart av trening med trening på høy intensitet for å utelukke risiko for iskemi og eventuelt arytmi.
Konklusjon
Flere studier har vist at intradialytisk styrke- og utholdenhetstrening kan gi pasienter med kronisk nyresvikt i endestadiet økt fysisk yteevne og bedret helserelatert livskvalitet.
Til tross for økende evidens relatert til effekter av trening og publiserte data fra K/DOQI (24) som stadfester at «alle dialysepasienter bør bli veiledet og regelmessig oppfordret av nefrolog og personalet på dialyseavdelingen om å øke fysisk aktivitetsnivå», er trening ikke en del av behandlingen til dialysepasienter i Norge. Fysioterapeutens rolle i en dialyseavdeling er ifølge artikkelforfatterne av stor betydning, og vi som faggruppe bør være mer proaktive i dette arbeidet. Pilotstudien utført ved dialyseavdelingen, Ullevål, i 1997 støtter opp under dette synet (25). I Sverige har flere dialyseavdelinger egne treningsrom i tilknytning til dialysen og pasientene oppfordres til, og det tilrettelegges for, at dialysepasientene kan være fysisk aktive under veiledning av fysioterapeut.
Referanser
1. Helsedirektoratet. Handlingsplan for forebygging og behandling av kronisk nyresykdom. In: Helsedirektoratet, editor.: Helsedirektoratet; 2011. p. IS-1884.
2. Hartmann AJ, T. Julsrud, J. Nyremedisin: en praktisk veileder. Oslo: Gyldendal Akademisk; 2008.
3. The Norwegian Renal Registry. Annual report 2012. 2012.
4. Hartmann A, Holdaas H, Os I, Hunderi O, Hallan S, Widerøe T, et al. Stadieinndeling og måling av nyrefunksjon ved kronisk nyresykdom. Tidsskr Nor Lægeforen 2006;126(9):1198-200.
5. Heiwe SM, K. Nyresykdom og nyretransplantasjon. In: Bahr R, editor. Aktivitetshåndboken Fysisik aktivitet i forebygging og behandling. s438-453. Oslo: Helsedirektoratet; 2008.
6. Jacobsen D, Kjeldsen SE, Ingvaldsen B, Lund K, Solheim K. Sykdomslære: indremedisin, kirurgi og anestesi. Oslo: Gyldendal Akademisk; 2009.
7. Cheema B, Abas H, Smith B, O’Sullivan A, Chan M, Patwardhan A, et al. Randomized controlled trial of intradialytic resistance training to target muscle wasting in ESRD: the Progressive Exercise for Anabolism in Kidney Disease (PEAK) study. American journal of kidney diseases : the official journal of the National Kidney Foundation. 2007 Oct;50(4):574-84. PubMed PMID: 17900457.
8. Johansen KL, Painter PL, Sakkas GK, Gordon P, Doyle J, Shubert T. Effects of resistance exercise training and nandrolone decanoate on body composition and muscle function among patients who receive hemodialysis: A randomized, controlled trial. Journal of the American Society of Nephrology : JASN. 2006 Aug;17(8):2307-14. PubMed PMID: 16825332.
9. Segura-Orti E. [Exercise in haemodyalisis patients: a literature systematic review]. Nefrologia : publicacion oficial de la Sociedad Espanola Nefrologia. 2010;30(2):236-46. PubMed PMID: 20098466. Ejercicio en pacientes en hemodialisis: revision sistematica de la literatura.
10. van Vilsteren MC, de Greef MH, Huisman RM. The effects of a low-to-moderate intensity pre-conditioning exercise programme linked with exercise counselling for sedentary haemodialysis patients in The Netherlands: results of a randomized clinical trial. Nephrology, dialysis, transplantation : official publication of the European Dialysis and Transplant Association - European Renal Association. 2005 Jan;20(1):141-6. PubMed PMID: 15522901.
11. Ouzouni S, Kouidi E, Sioulis A, Grekas D, Deligiannis A. Effects of intradialytic exercise training on health-related quality of life indices in haemodialysis patients. Clinical rehabilitation. 2009 Jan;23(1):53 63. PubMed PMID: 19114437.
12. Heiwe S, Tollin H. Patients’ perspectives on the implementation of intra-dialytic cycling-a phenomenographic study. Implementation science : IS. 2012;7:68. PubMed PMID: 22831388. Pubmed Central PMCID: 3444901.
13. Johansen KL. Exercise in the end-stage renal disease population. Journal of the American Society of Nephrology : JASN. 2007 Jun;18(6):1845-54. PubMed PMID: 17442789.
14. Clyne N. Motion förbetträr arbetsförmågan och muskelstyrkan vid kronisk njursvikt. Läkartidningen. 2004;101(50).
15. Clyne N, Jogestrand T, Lins LE, Pehrsson SK. Progressive decline in renal function induces a gradual decrease in total hemoglobin and exercise capacity. Nephron. 1994;67(3):322- 6. PubMed PMID: 7936023.
16. Akiba T, Matsui N, Shinohara S, Fujiwara H, Nomura T, Marumo F. Effects of recombinant human erythropoietin and exercise training on exercise capacity in hemodialysis patients. Artif Organs. 1995 Dec;19(12):1262-8. PubMed PMID: 8967886.
17. Borg G. Psychophysical scaling with applications in physical work and the perception of exertion. Scandinavian journal of work, environment & health. 1990;16 Suppl 1:55-8. PubMed PMID: 2345867.
18. Painter P, Moore G, Carlson L, Paul S, Myll J, Phillips W, et al. Effects of exercise training plus normalization of hematocrit on exercise capacity and health-related quality of life. American journal of kidney diseases : the official journal of the National Kidney Foundation. 2002 Feb;39(2):257-65. PubMed PMID: 11840365.
19. Parsons TL, Toffelmire EB, King-VanVlack CE. The effect of an exercise program during hemodialysis on dialysis efficacy, blood pressure and quality of life in end-stage renal disease (ESRD) patients. Clinical nephrology. 2004 Apr;61(4):261-74. PubMed PMID: 15125032.
20. Chen JL, Godfrey S, Ng TT, Moorthi R, Liangos O, Ruthazer R, et al. Effect of intra-dialytic, low-intensity strength training on functional capacity in adult haemodialysis patients: a randomized pilot trial. Nephrology, dialysis, transplantation : official publication of the European Dialysis and Transplant Association - European Renal Association. 2010 Jun;25(6):1936-43. PubMed PMID: 20100734. Pubmed Central PMCID: 2902890.
21. Cheema B, Abas H, Smith B, O’Sullivan A, Chan M, Patwardhan A, et al. Progressive exercise for anabolism in kidney disease (PEAK): a randomized, controlled trial of resistance training during hemodialysis. Journal of the American Society of Nephrology : JASN. 2007 May;18(5):1594-601. PubMed PMID: 17409306.
22. Stehman-Breen CO, Sherrard DJ, Alem AM, Gillen DL, Heckbert SR, Wong CS, et al. Risk factors for hip fracture among patients with end-stage renal disease. Kidney international. 2000 Nov;58(5):2200-5. PubMed PMID: 11044242.
23. Alem AM, Sherrard DJ, Gillen DL, Weiss NS, Beresford SA, Heckbert SR, et al. Increased risk of hip fracture among patients with end-stage renal disease. Kidney international. 2000 Jul;58(1):396-9. PubMed PMID: 10886587.
24. Workgroup KD. K/DOQI clinical practice guidelines for cardiovascular disease in dialysis patients. American journal of kidney diseases : the official journal of the National Kidney Foundation. 2005 Apr;45(4 Suppl 3):S1-153. PubMed PMID: 15806502.
25. Graver V, Stenehjem A, Biehl A. Should patients with chronic kidney failure exercise? – a pilot study. Fysioterapeuten. 1997;64(6):8-10

























