En systematisk oversiktsartikkel
Effekt av landbasert treningsterapi for pasienter med hofteleddsartrose
Vitenskapelig artikkel i Fysioterapeuten 5/2014.
Fredrik Paulsberg, turnusfysioterapeut, Ørsta kommune. Fredrik@paulsberg.com.
Stian Endre Olsen, turnusfysioterapeut, Rana kommune.
Håvard Østerås, førstelektor, studieleder og spesialist i idrettsfysioterapi. Fysioterapeututdanningen, Høgskolen i Sør-Trøndelag, Trondheim.
Denne vitenskapelige artikkelen er fagfellevurdert etter Fysioterapeutens retningslinjer. Akseptert 21.2.2014. Ingen interessekonflikter foreligger.
Sammendrag
Bakgrunn/hensikt: Artrose er en relativt vanlig sykdom, med en prevalens mellom en til 11 prosent i vest-europeiske land. Artrose kan forårsake smerte, stivhet, instabilitet, muskelsvakhet og redusert bevegelighet, noe som bidrar til nedsatt funksjon. Sykdommen reduserer mulighetene for en aktiv livsstil, og dermed pasientens opplevelse av livskvalitet. Denne studien undersøkte hvilken effekt landbasert treningsterapi kan ha på smerte, funksjon og livskvalitet hos pasienter med hofteleddsartrose.
Metode: Systematiske litteratursøk ble gjennomført i PubMed, CINAHL, EMBASE og PEDro for å finne RCT-studier gjort på treningsterapi ved hofteleddsartrose. Kvaliteten av hver enkelt artikkel ble undersøkt og klassifisert ved bruk av PEDro scale.
Resultater: Fem artikler passet kriteriene for inklusjon (n=549). Disse viste en moderat reduksjon i smerte og en moderat bedring i funksjon hos pasientene. Ingen statistisk signifikante forskjeller på livskvalitet ble funnet.
Konklusjon: Landbasert treningsterapi har moderat effekt på smerte og funksjon, men uten vedlikehold forsvinner effekten gradvis etter endt intervensjon. Hva som skal til for å få en større langtidseffekt bør undersøkes av fremtidige studier.
Nøkkelord: Artrose, treningsterapi, hofte, landbasert.
Innledning
Artrose er en degenerativ sykdom som kan forekomme i ethvert synovialt ledd og forårsake smerte, muskelsvakhet, redusert bevegelighet, stivhet og instabilitet, noe som bidrar til nedsatt funksjon (1, 2, 3). De vanligste leddene som rammes er hånd, knær og hofter. Sykdommen reduserer mulighetene for en aktiv livsstil, og dermed pasientens opplevelse av livskvalitet (1, 3, 4). Det er ofte varierende korrelasjon mellom patologiske funn, funksjonstap, livskvalitet og smerte (3, 5). I 2011 var det i alt 14 588 døgnopphold ved norske somatiske sykehus som følge av artrosetilstander, noe som tilsvarer ca. 1,7 prosent av alle døgnopphold totalt sett (6). Med prevalens mellom 1-11 prosent i vest-europeiske land (23), er artrose en relativt vanlig sykdom som krever betydelige mengder ressurser fra helsevesenet.
Det er erkjent at artrose er et sammensatt problem (5), og det er publisert en rekke europeiske anbefalinger for håndtering av artrose (5, 26, 30). Lohmander og Roos (7) angir rådgivning, hjelpemidler, fysioterapi, vektreduksjon, medikamenter og kirurgi som de vanligste behandlingsalternativene. Fysioterapeutenes bidrag er i stor grad treningsterapi og øvelsesbehandling, og i den kliniske hverdagen praktiseres dette ofte på land (landbasert trening). Treningsterapi er et vidt begrep og defineres som «en behandling eller en plan for fysisk aktivitet utformet og foreskrevet for spesifikke terapeutiske mål. Dens formål er å gjenopprette normal muskel- og skjelettfunksjon eller å redusere smerte forårsaket av sykdommer eller skader» (34, oversatt til norsk). Treningsterapi-begrepet begrenses altså ikke til konkrete konsepter rundt trening, som f. eks medisinsk treningsterapi.
Store kliniske retningslinjer anbefaler trening for pasienter med hofteleddsartrose (5, 26, 30), men resultatene fra randomiserte kontrollerte studier (RCT) tolkes forskjellig i systematiske oversiktsartikler og meta-analyser. McNair et al. (27) mener effekten ikke kan anslås på grunn av for lav dosering av intervensjonen, Hernandez-Molina et al. (28) hevder at treningsterapi er en effektiv behandling, mens Fransen et al. (29) og Fernandes et al. (30) påpeker at det ikke finnes studier av god nok kvalitet til verken å kunne avkrefte eller bekrefte effekten. Felles for tidligere oversiktsartikler/meta-analyser er inklusjon av flere typer treningsintervensjoner (land- og vannbasert, tai-chi og yoga), noe som kan underbygge motstridende resultater. Nytt for denne oversiktsartikkelen er inklusjonen av utelukkende landbaserte intervensjoner designet av profesjonelt helsepersonell.
Hensikt og spørsmål
Hensikten med denne oversiktsartikkelen er å gi fysioterapeuter oppdatert kjennskap til vitenskapelig dokumentert effekt av landbasert treningsterapi for pasienter med hofteleddsartrose. Effekten vurderes ut fra endret smerteopplevelse, kroppsfunksjon og livskvalitet. Det er utenfor denne artikkelens hensikt å sammenligne landbasert treningsterapi med effekten av andre lignende intervensjoner.
Metode
Søkestrategi
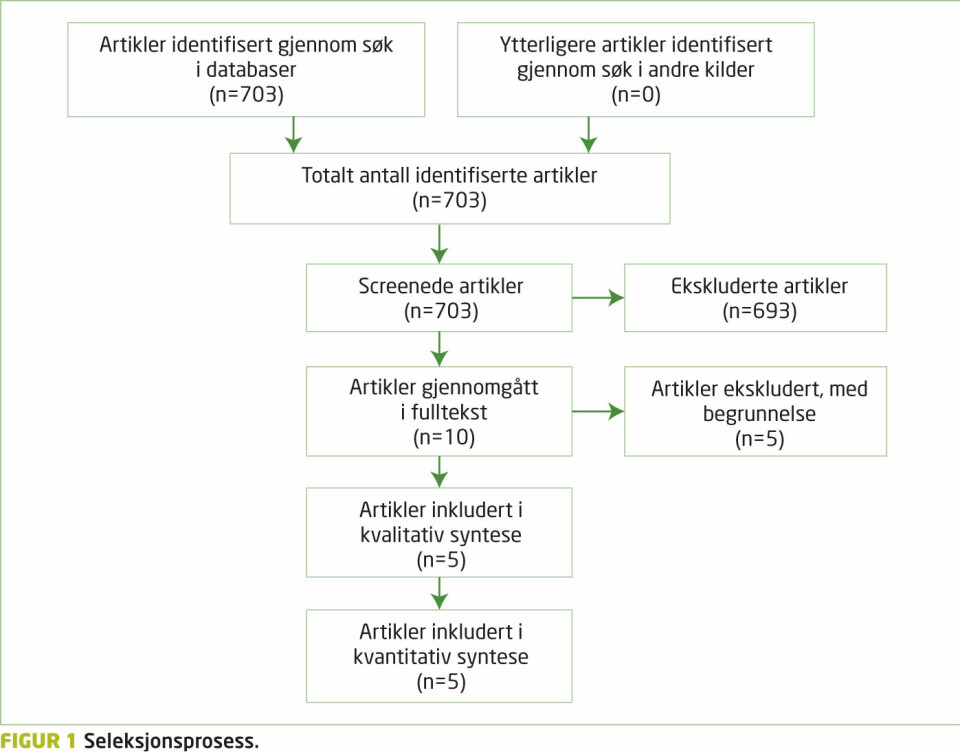
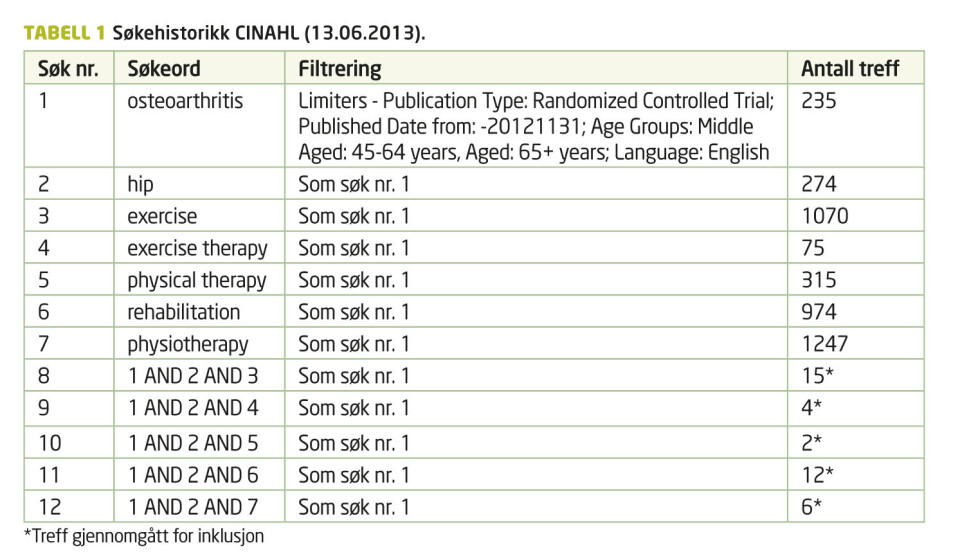
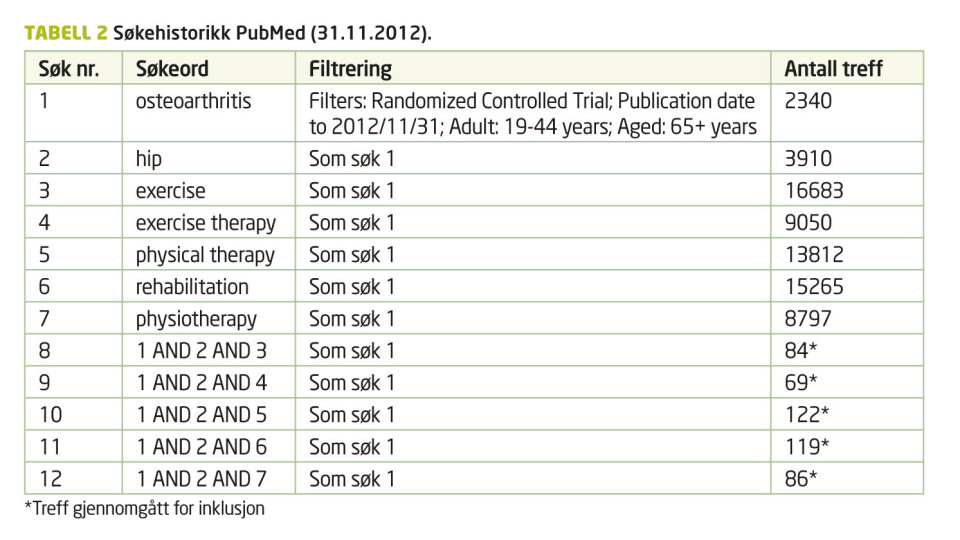
Forfatterne søkte etter artikler i databasene PubMed, CINAHL, EMBASE og PEDro med publiseringsdato før 31. november 2012. Detaljert beskrivelse av søkeprosessen i de enkelte databasene kan leses i tabell 1, 2, 3 og 4. Søkestrategien er tilpasset den enkelte database og kriteriene i avsnittene nedenfor er lagt til grunn.
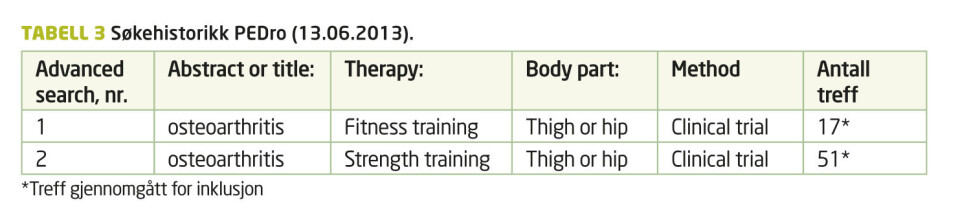
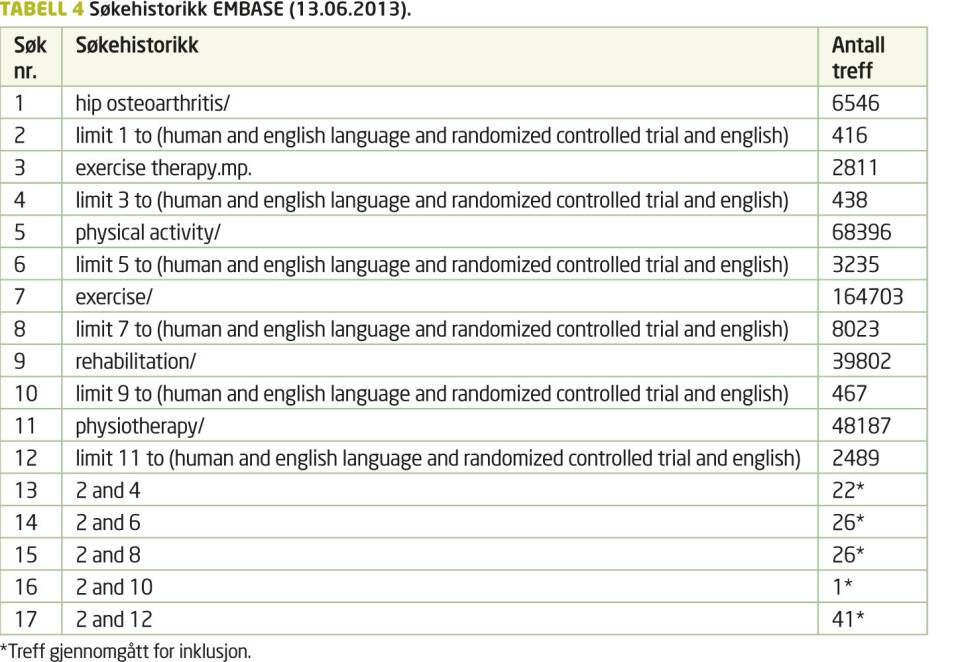
Type studier
Inkluderte studier skulle være fagfellevurderte RCT-studier, som sammenlignet en form for landbasert treningsterapi med en gruppe som ikke trener. Artiklene måtte være nordisk- eller engelskspråklige.
Type intervensjon
Landbasert treningsterapi for hofteleddsartrose, etter definisjonen som nevnt i innledningen. Treningen skulle vare minimum fire uker og være ledet av profesjonelt helsepersonell.
Pasientgruppe
Studiedeltakerne måtte ha diagnostisert artrose i hofteleddet, og det skulle ikke være planlagt eller gjennomført proteseoperasjon. Videre skulle studiene inneholde både kvinner og menn, og pasientene måtte være eldre enn 45 år.
Utfallsmål
I henhold til internasjonal konsensus på utfallsmål i kliniske forsøk på artrose i hånd, kne eller hofte (31), skulle studiene inneholde minst to av tre følgende utfallsmål:
fysisk funksjon (enten selvrapportert eller testet)
smerte
livskvalitet
Begrunnelse for inklusjon av studier
For å sammenligne effekten av treningsterapi med naturlig forløp, kunne ikke kontrollgruppen motta treningsterapi. Videre vil sannsynligvis ikke en treningsperiode på under fire uker gi grunnlag for å vurdere effekt av treningsterapi (3). Dette underbygges av at de fleste studier på treningsterapi, både hos friske og pasienter, varer i åtte til 12 uker. Hjemmebaserte treningsopplegg er vanskelig å kvalitetssikre, samt fratar oss muligheten til å fastlegge optimalt innhold i en treningsintervensjon. Treningen skulle være landbasert, siden basseng er dyrt tilleggsutstyr som mange behandlere ikke har tilgang til. Pasienter med hofteleddsprotese havner ikke innenfor pasientgruppen og ble derfor ekskludert. Pasienter som venter på operasjon har blitt ekskludert på bakgrunn av motivasjonsfaktorer som mulig feilkilde. Pasientene skulle være over 45 år, siden yngre pasienter ofte har sekundær artrose. Artiklene skulle være nordisk- eller engelskspråklige på grunn av manglende ressurser til oversetting.
Dataekstraksjon
Hver for seg leste forfatterne tittel og sammendrag på artiklene i søk med under 150 treff. På bakgrunn av dette ble artiklene som samsvarte med inklusjonskriteriene lest i sin helhet av alle forfatterne, og i en felles avgjørelse enten forkastet eller inkludert. De inkluderte artiklene ble kontrollert for intern validitet med PEDro scale (13). Forfatterne vurderte alle artiklene hver for seg, og ved uenighet ble det diskutert frem en konsensus.
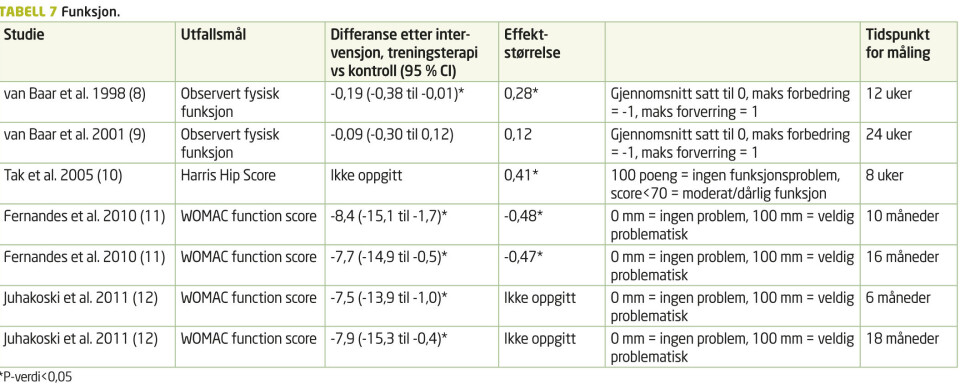
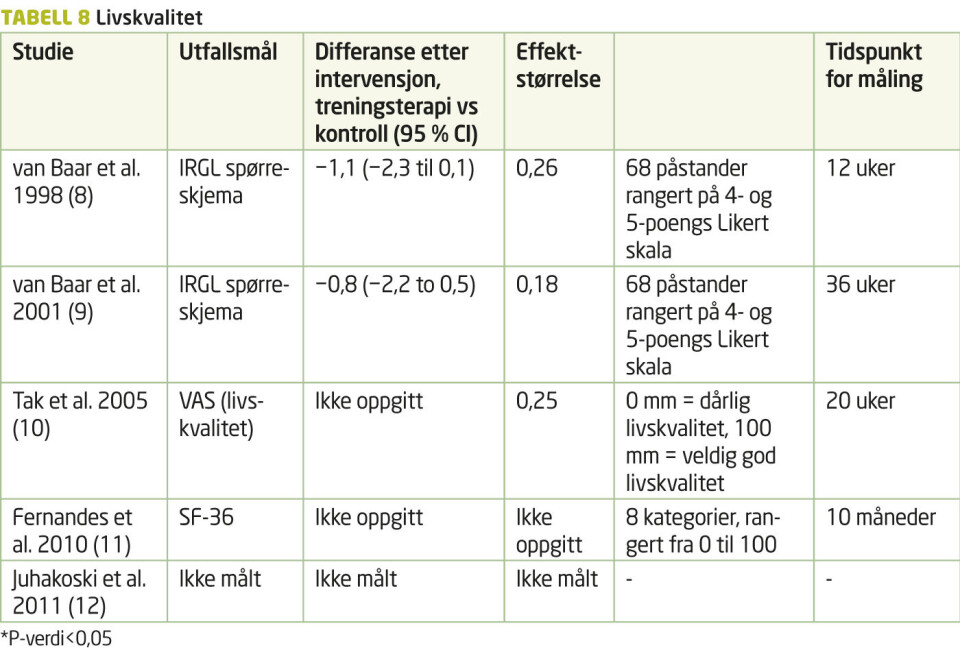
I fellesskap hentet forfatterne ut tallmateriale knyttet til smerte, funksjon og livskvalitet fra de inkluderte studiene. Dette er presentert i egne tabeller (tabell 6, 7 og 8). Innholdet i treningsintervensjonen ble hentet ut på samme måte, og presentert i tabell 9.
Dataanalyse
Effektstørrelser som er presentert i denne artikkelen ble hentet ut slik de var presentert i originalartiklene, og deretter brukt i vår samlede analyse. Der effektstørrelser ikke var tilgjengelig ble originalartiklenes confidence interval (CI) 95 % brukt som analysegrunnlag. På tross av forskjellige måleverktøy kan effektstørrelser gi et visst grunnlag for sammenligning på tvers av studier. Når det refereres til små (<0,2), moderate (rundt 0,5) og store effektstørrelser (>0,8) i denne artikkelen, tas det utgangspunkt i Cohens (15) kriterier for disse benevningene.
Effektstørrelsene i originalartiklene er presentert ved bruk av Cohens d. Effektstørrelsen blir dermed et resultat av differansen i mean-verdier dividert på disse resultatenes standard deviasjon. Metode for utregning av CI er ikke beskrevet i originalartiklene. P-verdier > 0.05, slik de er regnet ut av de publiserte artiklenes forfattere, ble vurdert til ikke signifikante resultater. Alle resultatene er mellom-gruppe-sammenligninger.
Resultater
Søkene i de ulike databasene ga til sammen 703 artikler hvor tittel og sammendrag ble gjennomgått. Blant disse ble ti artikler lest i sin helhet av alle forfatterne. Fem av artiklene (8, 9, 10, 11, 12) tilfredsstilte inklusjonskriteriene og ble dermed inkludert i oversiktsartikkelen. To av disse artiklene (8, 9) er samme studie, men de presenterer to forskjellige oppfølgingstidspunkter. Dette resulterte i et totalt antall pasienter n = 549. Søk etter eventuelle upubliserte studier ga ingen relevante treff.
Målingene av intern validitet på PEDro scale (13) viser at artiklene jevnt over holder høy kvalitet, med en score på 7 eller høyere (tabell 5). Alle studiene har gode, sammenlignbare grupper ved baseline og en tilfredsstillende mengde pasienter til oppfølgingsmålinger. Randomisering og evaluering av data er foretatt på en adekvat måte. Den eneste artikkelen som mangler skjult randomisering er Tak et al. (10). Alle artiklene manglet terapeut- og pasientblinding. De inkluderte studiene hadde baselinemålinger som baserte seg på preintervensjonsdata fra uke null, altså samme uke som intervensjonen begynte. Frekvens og antall punkter for oppfølgingsmålinger varierte.
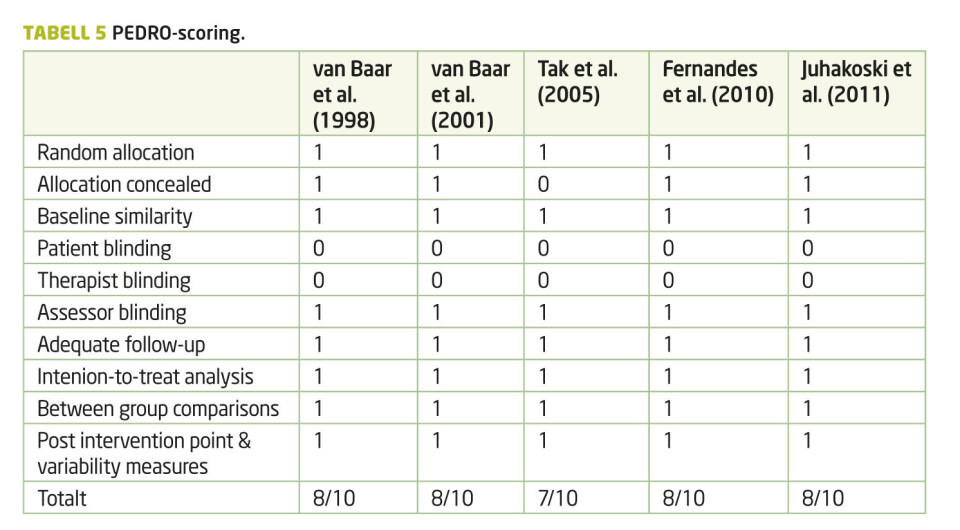
Alle studienes forfattere foruten Juhakoski et al. (12) har regnet ut effektstørrelser. Effektstørrelsene som presenteres for Fernandes et al. (11) angis med negativt fortegn dersom det var et positivt resultat for intervensjonsgruppen, siden dette var gjort i originalartikkelen. Det bør poengteres at van Baar et al. (8, 9) har inkludert pasienter som har artrose i hofte- og kneleddet. Artiklene ble likevel tatt med, da de tydelig poengterte at resultatene for hofte- og knepasienter var like, og derfor ble heller ikke resultatene delt opp for de to ulike diagnosegruppene i deres artikler.
Tre av studiene (8, 9, 10) fant signifikante forskjeller mellom gruppene i sine smertemål, og samtlige av disse var i fordel intervensjonsgruppen. Utfallsmålene er selvrapportert. Der fant van Baar et al. (8, 9) moderat effektstørrelse på VAS smerte siste uken (0.58 ved 12 uker og 0.36 ved 24 uker), og Tak et al. (10) moderat effektstørrelse på Harris Hip Score (0.51 ved åtte uker, 0.38 ved 20 uker), samt liten effektstørrelse på VAS smerte siste måned (0.17 ved 20 uker). Resultatene til Fernandes et al. (11) og Juhakoski et al. (12) manglet statistisk signifikans. Likevel ser man hos disse en tendens til nedgang i smerte i gjennomsnitt, og en noe større nedgang hos de som mottok treningsterapi. Tre av studiene (8, 9, 12) viser også til nedgang i bruk av paracetamol og/eller NSAIDs.
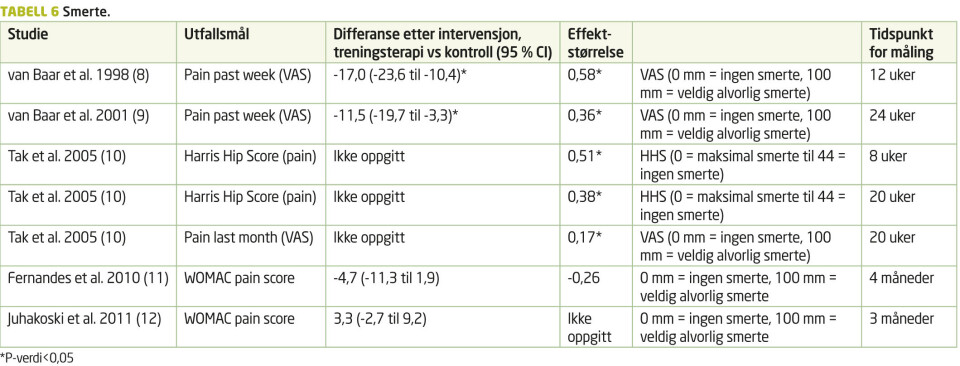
Det bør nevnes at forskjellige farmakologiske intervensjoner (opioider, glukosamin) har vist større effektstørrelser på smertereduksjon (henholdsvis 0.78 og 0.58) for pasienter med hofteleddsartrose (26).
Fire av fem studier (8, 10, 11, 12) viste signifikant fremgang i funksjon, både på objektive målinger (8, 10) og selvrapportert funksjon (10, 11, 12). van Baar et al. (8) fant moderat bedring i observert funksjon (0,28 ved åtte uker) og Tak et al. (10) moderat effekt på Harris Hip Score (0,41 ved åtte uker). Fernandes et al. (11) fant moderat bedring i WOMAC function score (-0,48 ved 10 mnd, -0,47 ved 16 mnd). Juhakoski et al. (12) kan vise til en gjennomsnittlig bedring i WOMAC function score (95 % CI; -7,5 (-13,9 til -1,0) ved 6 mnd, -7,9 (-15,3 til -0,4) ved 18 mnd). van Baar et al. (9) er den eneste studien som ikke viser signifikant fremgang.
Når det gjelder målingene gjort på livskvalitet, finnes det ingen statistisk signifikante resultater (P-verdier > 0.05).
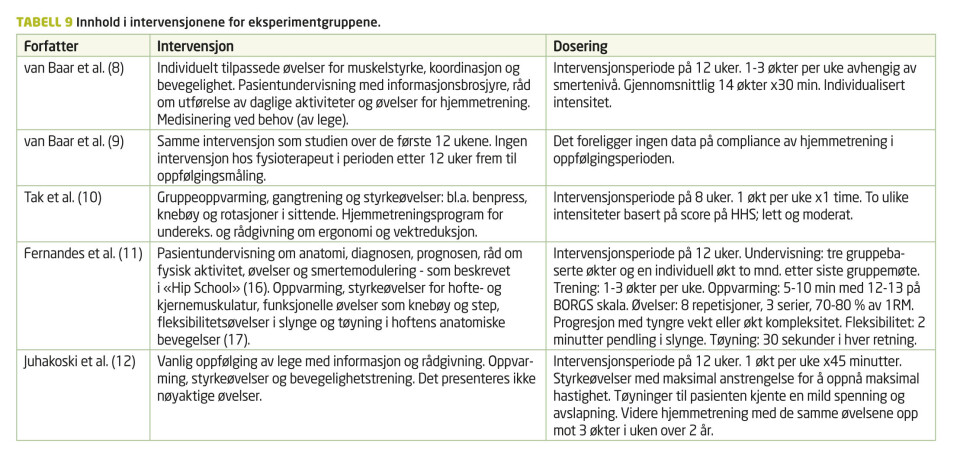
Når det gjelder intervensjonen/treningen som er gjort, spriker det veldig i innhold og dosering. I tabell 9 presenteres den informasjonen som kunne hentes ut av artiklene om intervensjonen. Manglende beskrivelse fra forfatterne er i hovedsak det som gjør uthenting av spesifikk informasjon om treningsopplegget vanskelig.
Diskusjon
Etter søk i relevante databaser passet fem studier (8, 9, 10, 11, 12) med inklusjonskriteriene for denne oversiktsartikkelen. De inkluderte studiene viste moderat reduksjon i smerte og moderat bedring i funksjon hos pasientene. Når det gjelder livskvalitet, har ingen av studiene statistisk signifikante resultater.
Metodekritikk
Dette er den første oversiktsartikkelen som tar for seg utelukkende landbasert treningsterapi. På grunn av dette var inklusjons- og eksklusjonskriteriene strenge, noe som kan forklare et relativt lavt antall artikler.
Virkningsmekanismene bak landbasert treningsterapi og vannbasert treningsterapi er forskjellige, og med bakgrunn i dette bør man ikke analysere disse intervensjonene samlet. Det er derfor av klinisk interesse å skille disse to.
En svakhet i metoden er at oversiktsartikkelen er begrenset til nordisk- og engelskspråklige artikler. Det kan finnes flere gode artikler på treningsterapi ved hofteleddsartrose som har blitt skrevet på et annet språk. Forfatterne av denne oversiktsartikkelen var heller ikke blindet med tanke på hvilke tidsskrift som har publisert og hvilke forfattere som har skrevet artiklene. Dette kan ha gjort tolkningen av resultatene mindre objektiv, og ført til større usikkerhet (14).
Intern validitet
Tak et al. (10) kan ikke krediteres for skjult randomisering, da metodebeskrivelsen ikke er dekkende. Dersom personen som avgjorde om pasienten var skikket for inklusjon allerede var klar over hvilken gruppe pasienten havnet i, vil dette kunne påvirke avgjørelsen om pasienten skulle være med på studien. Dette understøttes av Schulz et al. (18), som har funnet empirisk evidens for at manglende skjult randomisering er assosiert med usikkerhet. I tillegg manglet alle studiene blinding av både terapeuter og pasienter. Dette kan påvirke terapeutenes oppførsel, slik at de diskriminerer pasienten i favør den gruppen de ønsker skal ha mest fremgang. Manglende pasientblinding kan altså føre til usikkerhet gjennom blant annet økt placebo-, nocebo- og Hawthorne-effekt (32).
Baselineverdiene i alle studiene er innhentet i uke null. Siden artrose er en sykdom preget av et svingende sykdombilde (5), ville det vært hensiktsmessig å ha en baseline som ga oss informasjon om pasientene var i en god eller dårlig periode før intervensjonen.
Resultatdiskusjon
Denne oversiktsartikkelen fokuserer på utfallene smerte, funksjon og livskvalitet hos pasientene i de inkluderte studiene. Tabell 10 viser at alle de inkluderte studiene finner fordeler med å motta treningsterapi, om enn basert på noe ulike effektmål.
De statistisk signifikante resultatene (8, 9, 10) på studienes smertemålinger virker å være positive i favør intervensjonsgruppen, men med moderate effektstørrelser. Dette har klinisk relevans siden smerte er et av de vanligste symptomene ved hofteleddsartrose (1, 2, 3, 31). Videre ser man at effekten avtar over tid (tabell 6), noe som underbygger at treningen må vedlikeholdes utover en intervensjonsperiode. I klinisk sammenheng har dette stor betydning, da man må opprettholde aktiviteten for å holde smertereduksjonen ved like, og at det foreløpig ikke foreligger en dokumentert treningsintervensjon som permanent reduserer smerten uten spesifikk oppfølging. Andre studier viser også trening som en effektiv smertemodulator både akutt og en tid etter avsluttet økt hos pasienter med kroniske lave ryggsmerter (19). For kroniske smertepasienter virker regelmessig trening smertereduserende (20).
Funksjonsgevinsten av treningsterapi viser seg positiv i fire av artiklene, med moderat effektstørrelse (8, 10, 11, 12). Både Juhakoski et al. (12) og Fernandes et al. (11) kan vise til bedring av funksjon, uten at de har statistisk signifikant smertereduksjon. Klinisk sett kan dette bety at pasienter med hofteleddsartrose lettest får gevinst på funksjonsnivå, uten at de nødvendigvis får en smertereduksjon samtidig. Det ser også ut til at effekten avtar over tid, siden funksjonsgevinsten forsvinner ved oppfølgingsmålinger. Unntaket er Juhakoski et al. (12), hvor de finner selvrapportert funksjonsgevinst også etter 18 mnd. Dette kan forklares av at deres intervensjon hadde fire såkalte «boosterøkter» ett år etter den opprinnelige treningsperioden. Resultatene samsvarer med forskning som er gjort på friske pasienter, som viser at man må vedlikeholde trening for å ha et langvarig utbytte på funksjonsnivå (21).
Ingen av studiene kunne vise til at deres intervensjon hadde signifikante endringer av pasientenes livskvalitet. Dette kan skyldes bruk av manglende sensitive måleinstrumenter som oppfatter den bedringen som kan være til stede. Rajagopalan et al. (22) underbygger denne påstanden ved å vise at generelle livskvalitetsskjema var mindre valid for deres pasienter enn sykdomsspesifikke skjema.
Konklusjonene fra tidligere oversiktsartikler (27-30, 35) på dette emnet spriker mye. Felles for disse artiklene er et relativt lavt antall originalartikler (<10). Likevel ser det ut til at funnene er i tråd med det vi presenterer i denne studien når det kommer til smerte og funksjon, også med tanke på effektstørrelser. Siden disse studiene også har inkludert andre former for trening (tai chi, yoga, vannbasert trening), kan det tenkes at treningsform ikke er meget relevant for effekten.
Det er forskjeller mellom studiene når det kommer til innhold i treningsintervensjonen. Informasjonen som er gitt til pasientene er relativt lik på tvers av studiene. Alle studiene har gitt intervensjonsgruppen oppvarming og treningsterapi, men nøyaktig hvilke øvelser pasientene har gjennomført er vanskelig å fastslå på grunn av mangelfull informasjon i artiklene. Studiene sier oss altså ingenting om hvilke øvelser eller hvilken type treningsterapi (globale øvelser, øvelsesbehandling eller bevegelighetstrening) som gir resultater, men bare at det gir positive resultater som en samlet kointervensjon. Det ser ut til at det mangler studier som evaluerer treningsprogrammer for hofteleddsartrose, noe som Tak et al. (10) påpeker.
I likhet med øvelsesutvalget spriker det også når det gjelder dosering av treningsterapien (tabell 9). Angående varighet og hyppighet på hver enkelt økt, har studiene lagt seg på en relativt lav belastning for pasientene. Det må påpekes at dette kan være for lavt dosert til å få fremgang i løpet av intervensjonsperioden. Dette underbygges av anbefalingene i Physical Activity Guidelines Advisory Committee Report (33), som sier at pasienter med artrose bør være i minst 150 minutter moderat- eller 75 minutter høy-intensiv aktivitet i løpet av en uke. Ingen av studiene møter disse kravene, og dette kan være grunnen til at resultatene i denne studien er lite overbevisende sammenlignet med anbefalingene for håndtering av hofteleddsartrose (5, 26, 30).
Forskjellene i intensitet i treningsprogrammene er store (tabell 9). For eksempel instruerte Juhakoski et al. (12) pasientene til å trene med maksimal anstrengelse og maksimal hastighet, mens Tak et al. (10) instruerte i noe de kaller lett til moderat intensitet, hvor de ikke oppgir antall repetisjoner eller serier. Det er heller ikke skrevet noe om hvordan det er tatt hensyn til smerte og andre symptomer. Det forfatterne kan se ut fra denne analysen er altså ikke hvilken dosering som gir best resultater, men bare at treningsterapi på generell basis gir effekt.
Det er gjort studier med tydelige funn på at dosering har betydning for resultatet av opptreningen hos mange pasientgrupper med langvarige smerter, blant annet hos pasienter med patellofemoralt smertesyndrom (24) og langvarig subacromial smerte (25). Disse studiene har vist positive resultater i favør høydosert treningsterapi sammenlignet med mer tradisjonell lavdosert treningsterapi, særlig med tanke på langtidseffekt. Muligens foreligger det lignende forhold hos pasienter med hofteleddsartrose. Videre forskning bør studere dose-responsforholdet av treningsterapi for pasienter med hofteleddsartrose.
I de overnevnte studiene (24, 25) er øvelsesutvalget og doseringen standardisert. Pasientene ble gradvis eksponert for økende dosering, hvor man ikke ønsket å forverre pasientens symptomer. På denne måten kan man ivareta individualiseringen av et øvelsesprogram, samtidig som man har standardisert øvelser og dosering.
Konklusjon
Landbasert treningsterapi har moderat effekt på smerte og funksjon hos pasienter med hofteleddsartrose. Det fantes ingen statistisk signifikante resultater på målingene av livskvalitet. Effekten ser ut til å være størst rett etter avsluttet intervensjon, deretter avtar effekten over tid. Hva som skal til for å få en større langtidseffekt bør undersøkes av fremtidige studier.
Referanseliste
1. Dekker J, Boot B, van der Woude LH, Bijlsma JW (1992). Pain and disability in osteoarthritis: a review of biobehavioral mechanisms. J Behav Med., 15, 189–214.
2. Arokoski MH, Haara M, Helminen HJ, Arokoski JP. (2004). Physical function in men with and without hip osteoarthritis. Arch Phys Med Rehabil., 85, 574-581.
3. Vogels EMHM, Hendriks HJM, van Baar ME, Dekker J, Hopman-Rock M, Oostendorp RAB, Hullegie WAMM, Bloo H, Hilberdink WKHA, Munneke M, Verhoef J. (2003). Clinical practice guidelines for physical therapy in patients with osteoarthritis of the hip or knee. Hentet fra http://www.ifompt.com/site/ifompt/files/pdf/Osteoarthr.H-K.Gln.pdf
4. van Baar ME, Dekker J, Lemmens JA, Oostendorp RA, Bijlsma JW. (1998). Pain and disability in patients with osteoarthritis of hip or knee: the relationship with articular, kinesiological, and psychological characteristics. J Rheumatol., 25, 125–133.
5. National Collaborating Centre for Chronic Conditions. (2008). Osteoarthritis: national clinical guideline for care and management in adults. Royal College of Physicians. London.
6. Statistisk sentralbyrå – «Døgnopphold ved somatiske sykehus, etter alder og hoveddiagnose. 2011». (2011). Hentet 13. november 2012 fra http://www.ssb.no/emner/03/02/pasient/tab-2012-04-20-01.html
7. Lohmander LS, Roos EM. (2007). Clinical update: treating osteoarthritis. Lancet, 370, 2082-2084.
8. van Baar ME, Dekker J, Oostendorp RA, Bijl D, Voorn TB, Lemmens JA, Bijlsma JW. (1998). The effectiveness of exercise therapy in patients with osteoarthritis of the
hip or knee: a randomized clinical trial. J Rheumatol., 25 Dec (12), 2432-2439.
9. van Baar ME, Dekker J, Oostendorp RA, Bijl D, Voorn TB, Bijlsma JW. (2001). Effectiveness of exercise in patients with osteoarthritis of hip or knee: nine months’ follow up. Ann Rheum Dis., Dec, 60(12), 1123-1130.
10. Tak E, Staats P, Van Hespen A, Hopman-Rock M. (2005). The effects of an exercise program for older adults with osteoarthritis of the hip. J Rheumatol., 32, Jun (6), 1106-1113.
11. Fernandes L, Storheim K, Sandvik L, Nordsletten L, Risberg MA. (2010). Efficacy of patient education and supervised exercise vs patient education alone in patients with hip osteoarthritis: a single blind randomized clinical trial. Osteoarthritis Cartilage, 18, Oct (10), 1237-1243.
12. Juhakoski R, Tenhonen S, Malmivaara A, Kiviniemi V, Anttonen T, Arokoski JP. (2011). A pragmatic randomized controlled study of the effectiveness and cost consequences of exercise therapy in hip osteoarthritis. Clin Rehabil., 25, Apr (4), 370-383.
13. PEDro scale. Hentet fra 8. mai 2013 fra http://www.pedro.org.au/wp-content/uploads/PEDro_scale.pdf
14. Kumar M. (2009). A review of the review process: manuscript peer-review in biomedical research. Biology and Medicine, 1(4), 1-16.
15. Cohen J. (1988) Statistical power of analysis for the behavioral sciences. Hillsdale, NJ: Lawrence Erlebaum Associates.
16. Klassbo M, Larsson G, Harms-Ringdahl K. (2003). Promising outcome of a hip school for patients with hip dysfunction. Arthritis Rheum., 49(3), 321-327.
17. Nordsletten L, Risberg MA. (2010). Development of a therapeutic exercise program for patients with osteoarthritis of the hip. Phys Ther., 90, Apr (4), 592-601.
18. Schulz KF, Chalmers I, Hayes RJ, Altman DG. (1995). Empirical evidence of bias. Dimensions of methodological quality associated with estimates of treatment effects in controlled trials. JAMA, 273, Feb 1(5), 408-412.
19. Hoffman MD, Shepanski MA, MacKenzie SP, Clifford PS. (2005). Experimentally induced pain perception is acutely reduced by aerobic exercise in people with chronic low back pain. Journal of Rehabilitation Research & Development, 42(2), 183-190.
20. Hoffman MD, Hoffman DR. (2007). Does Aerobic Exercise Improve Pain Perception and Mood? A Review of the Evidence Related to Healthy and Chronic Pain Subjects. Current Pain and Headache Reports, 11, 93–97.
21. American College of Sports Medicine Position Stand. (1998). The recommended quantity and quality of exercise for developing and maintaining cardiorespiratory and muscular fitness, and flexibility in healthy adults. Med Sci Sports Exerc., 30 Jun (6), 975-991.
22. Rajagopalan K, Abetz L, Mertzanis P, Espindle D, Begley C, Chalmers R, Caffery B, Snyder C, Nelson JD, Simpson T, Edrington T. (2005). Comparing the discriminative validity of two generic and one disease-specific health-related quality of life measures in a sample of patients with dry eye. Value Health, 8, Mar-Apr (2), 168-174.
23. Felson DT, Zhang Y. (1998). An update on the epidemiology of knee and hip osteoarthritis with a view to prevention. Arthritis Rheum., 41,1343–1355.
24. Østerås B, Østerås H, Torstensen TA, Vasseljen O. (2012). Dose-response effects of medical exercise therapy in patients with patellofemoral pain syndrome: a
randomised controlled clinical trial. Physiotherapy 99(2), 126-131.
25. Østerås H, Torstensen TA. (2010). The dose-response effect of medical exercise therapy on impairment in patients with unilateral longstanding subacromial pain. Open
Orthop J. 5(4), 1-6.
26. Zhang W, Nuki G, Moskowitz RW, Abramson S, Altman RD, Arden NK, Bierma-Zeinstra S, Brandt KD, Croft P, Doherty M, Dougados M, Hochberg M, Hunter DJ, Kwoh K, Lohmander LS, Tugwell P. (2010). OARSI recommendations for the management of hip and knee osteoarthritis Part III: changes in evidence following systematic cumulative update of research published through January 2009. Osteoarthritis Cartilage, 18(4), 476-499.
27. McNair PJ, Simmonds MA, Boocock MG, Larmer PJ. (2009). Exercise therapy for the management of osteoarthritis of the hip joint: a systematic review. Arthritis Res Ther., 11(3), R98.
28. Hernandez-Molina G, Reichenbach S, Zhang B, Lavalley M, Felson DT. (2008). Effect of therapeutic exercise for hip osteoarthritis pain: results of a meta-analysis. Arthritis Rheum., 59, 1221–1228.
29. Fransen M, McConnell S, Hernandez-Molina G, Reichenbach S. (2010). Does land-based exercise reduce pain and disability associated with hip osteoarthritis? A meta-analysis of randomized controlled trials. Osteoarthritis Cartilage, 18, May (5), 613-620.
30. Fernandes L, Hagen KB, Bijlsma JW, Andreassen O, Christensen P, Conaghan PG, Doherty M, Geenen R, Hammond A, Kjeken I, Lohmander LS, Lund H, Mallen CD, Nava
T, Oliver S, Pavelka K, Pitsillidou I, da Silva JA, de la Torre J, Zanoli G, Vliet Vlieland TP. (2013). European League Against Rheumatism (EULAR). EULAR recommendations for the non-pharmacological core management of hip and knee osteoarthritis. Ann Rheum Dis., 72(7), 1125-1135.
31. Bellamy N, Kirwan J, Boers M, Brooks P, Strand V, Tugwell P, Altman R, Brandt K, Dougados M, Lequesne M. (1997). Recommendations for a core set of outcome measures for future phase III cinical trials in knee, hip and hand osteoarthritis. Consesus development at OMERACT III. Journal of Rheumatology, 24(4), 799-802.
32. Nüesch E, Reichenbach S, Trelle S, Rutjes AW, Liewald K, Sterchi R, Altman DG, Jüni P. (2009). The importance of allocation concealment and patient blinding in
osteoarthritis trials: a meta-epidemiologic study. Arthritis Rheum. 61(12), 1633-1641.
33. Physical Activity Guidelines Advisory Committee. (2008). Physical Activity Guidelines Advisory Committee Report. Department of Health and Human Services. Washington DC.
34. PubMed MeSH – «Exercise Therapy» (u.å.) Hentet ut november 2013 fra http://www.ncbi.nlm.nih.gov/mesh/68005081.
35. Hernandez-Molina G, Reichenbach S, Zhang B, LaValley M, Felson D. (2008). Effect of Therapeutic Exercise for Hip Osteoarthritis Pain: Results of a Meta-Analysis. Arthritis Rheum. 59(9): 1221-1228























